Значение цветных реакций состоит в том, что они дают возможность обнаружить присутствие белка в биологических жидкостях, растворах и установить аминокислотный состав различных природных белков. Эти реакции применяются как для качественного, так и для количественного определения белка и содержащихся в нем аминокислот. Некоторые реакции присущи не только белкам, но и другим веществам, например, фенол, подобно тирозину, дает розово-красное окрашивание с реактивом Миллона, поэтому проведения одной какой-либо реакции для установления наличия белка не достаточно.
Существует два типа цветных реакций: 1) универсальные – биуретовая (на все белки) и нингидриновая (на все а -аминокислоты и белки); 2) специфические – только на определенные аминокислоты как в молекуле белка, так и в растворах отдельных аминокислот, например реакция Фоля (на аминокислоты, содержащие слабосвязанную серу), реакция Миллона (на тирозин), реакция Сакагучи (на аргинин) и др.
При проведении цветных реакций на белки и аминокислоты необходимо предварительно составить следующую таблицу:
Цветные реакции на белки (качественные реакции)
Цветные реакции на белки Опыт 1. Биуретовая реакция.
Биуретовая реакция – качественная на все без исключения белки , а также продукты их неполного гидролиза , которые содержат не менее двух пептидных связей .
Принцип метода. Биуретовая реакция обусловлена присутствием в белках пептидных связей (- СО – NH -), которые в щелочной среде образуют с сульфатом меди (ІІ) окрашенные в красно-фиолетовый цвет медные солеобразные комплексы . Биуретовую реакцию дают также некоторые небелковые вещества, например биурет (NH 2 -CO-NH-CO-NH 2), оксамид (NH 2 CO-CO-NH 2), ряд аминокислот (гистидин , серин , треонин , аспарагин ).
Биуретовая реакция с глицином
Порядок выполнения работы.
К 1 мл исследуемого 1% раствора белка добавляют равный объем 10 % раствора гидроксида натрия (NaOH) щелочи и затем 2-3 капли 1 % раствора сульфата меди (CuSO 4). разбавленного, почти бесцветного раствора медного купороса.
При положительной реакции появляется фиолетовая окраска с красным либо синим оттенком.
Опыт 2. Реакция на «слабосвязанную серу».
Принцип метода. Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Порядок выполнения работы.
В пробирку наливают 1 мл неразбавленного куриного белка, прибавляют 2 мл 20%-го раствора гидроксида натрия. Смесь осторожно кипятят (чтобы смесь не выбросило).
При этом выделяется аммиак, который обнаруживается по посинению влажной лакмусовой бумажки, поднесенной к отверстию пробирки (не касаться стенки). Образующийся незначительный осадок растворяется при кипении, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):


Химизм реакции:

|
черный осадок |
В пробирку наливают 1 мл. неразбавленного куриного белка добавляют 2 мл. концентрированного раствора щелочи, кладут несколько кипятильников. К горячему раствору добавляют раствор плюмбита натрия – образуется желто-бурое или черное окрашивание. (Плюмбит натрия готовят следующим образом: к 1 мл уксуснокислого свинца добавляют раствор щелочи по каплям до растворения образующего вначале осадка гидроксида свинца).
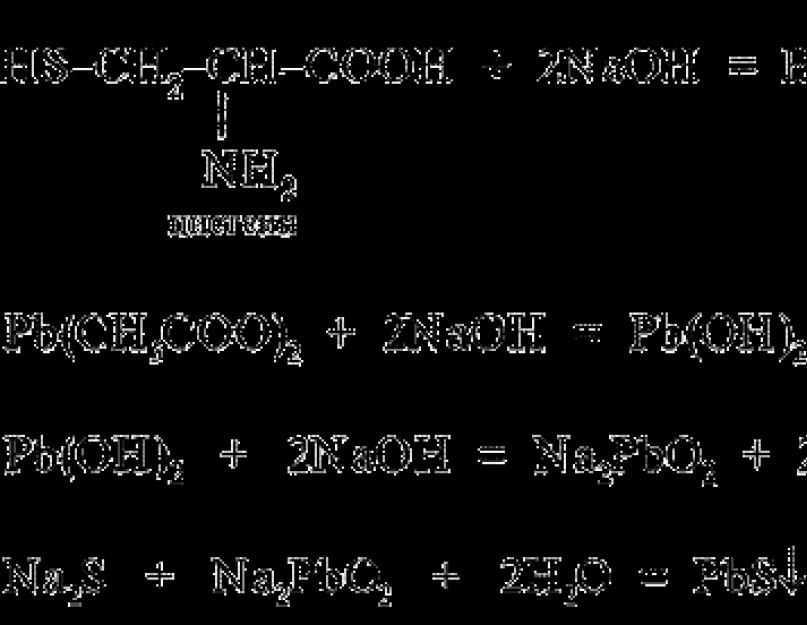
При наличии в молекуле белка серосодержащих аминокислот (цистина, цистеина) из этих аминокислот постепенно отщепляется сера в виде иона в степени окисления – 2, наличие которого и обнаруживается ионом свинца, образующим с ионом серы черный нерастворимый сульфид свинца:
Pb(CH 3 COO) 2 + 2NaOH Pb(OH) 2 + 2 CH 3 COONa,
Pb(OH) 2 + 2NaOH Na 2 PbO 2 + H 2 O,
Na 2 S + Na 2 PbO 2 + 2H 2 O PbS + 4NaOH.
Опыт 3. Ксантопротеиновая реакция белков.
Принцип метода. Эта реакция используется для обнаружения a-аминокислот, содержащих ароматические радикалы. Тирозин, триптофан, фенилаланин при взаимодействии с концентрированной азотной кислотой образуют нитропроизводные, имеющие желтую окраску. В щелочной среде нитропроизводные этих a-аминокислот дают соли, окрашенные в оранжевый цвет. Желатин, например, не содержащий ароматических аминокислот, не дает ксантопротеиновой пробы.
Порядок выполнения работы.
К 1 мл 10 %-го раствора белка куриного яйца добавляют 0,5 мл концентрированной азотной кислоты. В результате коагуляции белка в содержимом пробирки образуется белый осадок или помутнение. При нагревании раствор и осадок окрашиваются в ярко-желтый цвет. При этом осадок почти полностью растворяется в результате гидролиза. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия (до появления оранжевой окраски раствора).
Рассмотрим механизм ксантопротеиновой реакции по радикалу тирозина:


Химизм реакции :

Оформление опыта: сделать вывод и написать уравнение реакции.
Опыт 4. Реакция Адамкевича (на присутствие в белках триптофана).
Принцип метода. Белки, содержащие триптофан, в присутствии глиоксиловой и серной кислот дают красно-фиолетовое окрашивание. Реакция основана на способности триптофана взаимодействовать в кислой среде с альдегидами глиоксиловой кислоты (являющейся примесью к концентрированной уксусной кислоте) с образованием окрашенных продуктов конденсации. Реакция протекает по уравнению:

Желатин не дает этой реакции, т.к. он не содержит триптофана. Окраска возникает за счет реакции триптофана с глиоксиловой кислотой, всегда присутствующей в уксусной кислоте в виде примеси.
Эту же реакцию на триптофан можно провести, используя вместо уксусной кислоты формальдегид 2,5%-ный раствор концентрированной H 2 SO 4. Раствор перемешать и через 2-3 мин. добавить при взбалтывании 10 капель 5%-ного нитрита натрия. Развивается интенсивно-фиолетовое окрашивание, на этом основан принцип метода реакции.
Порядок выполнения работы.
В пробирку наливают несколько капель неразбавленного белка и прибавляют 2 мл. ледяной уксусной кислоты и несколько капель глиоксиловой кислоты. Смесь слегка нагревают до растворения образующегося осадка, охлаждают и, сильно наклонив пробирку, осторожно по стенке приливают концентрированную H 2 SO 4 так, чтобы обе жидкости не смешивались.
Через 5-10 минут на границе раздела двух слоев наблюдают образование красно-фиолетового кольца.
Опыт 5. Нингидриновая реакция.
Принцип метода. a-Аминокислоты реагируют с нингидрином, образуя сине-фиолетовый комплекс (пурпур Руэманна), интенсивность окраски которого пропорциональна количеству аминокислоты. Реакция идет по схеме:

Химизм реакции :


Реакция с нингидрином используется для визуального обнаружения a-аминокислот на хроматограммах (на бумаге, в тонком слое), а также для колориметрического определения концентрации аминокислот по интенсивности окраски продукта реакции.
Продукт этой реакции содержит в своем составе радикал (R) исходной аминокислоты, который обусловливает различную окраску: голубую, красную, и т.д. соединений, возникающих при реакции аминокислот с нингидрином.
В настоящее время нингидриновая реакция широко используется как для открытия отдельных аминокислот, так и для определения их количества.
Порядок выполнения работы.
В пробирку наливают 1 мл 1-10%-го разбавленного раствора белка куриного яйца и 1-2 мл 1%-го раствора нингидрина в ацетоне. Содержимое пробирки перемешивают и в течение 2-3 мин осторожно нагревают на водяной бане до появления сине-фиолетового окрашивания, свидетельствующее о присутствии в белке α -аминокислот.
Оформление опыта: сделать вывод и написать уравнение реакции.
Опыт 6. Реакция Сакагучи.
Принцип метода. Эта реакция на аминокислоту аргинин основана на взаимодействии аргинина с a-нафтолом в присутствии окислителя. Ее механизм еще полностью не выяснен. По-видимому, реакция осуществляется по следующему уравнению:

Поскольку производные хинониминов (в данном случае нафтохинона), у которых водород иминогруппы –NH– замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона, то, по-видимому, оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именно производного нафтохинонимина. Не исключена, однако, вероятность образования еще более сложного соединения за счет дальнейшего окисления оставшихся NH-групп аргининового остатка и бензольного ядра a-нафтола:
Порядок выполнения работы.
К 2 мл. 1%-го разбавленного раствора белка куриного яйца добавляют 2 мл. 10%-го гидроксида натрия (NaOH) и несколько капель 0,2%-ного спиртового раствора α -нафтола. Содержимое пробирки хорошо перемешивают. Затем приливают 0,5 мл. гипобромита натрия (NaBrO) или гипохлорита натрия (натрий хлорноватистокислый – NaOCl), перемешивают. Тотчас появляется красное, постепенно усиливающееся окрашивание.
Немедленно добавляют 1 мл 40%-го раствора мочевины для стабилизации, быстро развивающегося оранжево-красного окрашивания.
Эта реакция характерна для соединений, содержащих остаток гуанидина
NH = C –NH 2 ,
и указывает на присутствие в белковой молекуле аминокислоты-аргинина:
NH = C –NH – (CH 2) 3 –CH –COOH
Оформление опыта: сделать вывод и написать уравнение реакции.
Белок - самая важная составная часть пищи - основа всего живого, строительный материал всякого организма. Тысячи исследователей во всем мире работают с белком, изучают его свойства. Конечно, в наших опытах мы не откроем ничего нового. Но, говорят, лиха беда начало...
Первый опыт - качественная реакция на белок, т. е. такая реакция, которая позволит нам уверенно судить - белок перед нами или нет. Таких реакций несколько. Ту, которую мы проведем, называют биуретовой . Для нее нам потребуются растворы стиральной соды (или едкого натра) и медного купороса.
Приготовьте несколько растворов, которые, как можно предположить, содержат белок. Пусть это будет мясной или рыбный бульон (желательно процеженный через марлю), отвар каких-либо овощей или грибов и др. Растворы налейте в пробирки примерно наполовину. Затем прибавьте немного раствора щелочи - едкого натра или стиральной соды (раствор соды желательно прокипятить и остудить). Наконец, добавьте голубого раствора медного купороса. Если в испытуемом отваре действительно есть белок, то окраска сразу станет фиолетовой. Про такие реакции говорят, что они характерные . Они идут только в том случае, если в растворе действительно есть белок. Для контроля поставьте опыт с лимонадом или с минеральной водой.
Всем известно, что при нагревании белок свертывается и переходит в нерастворимую форму - сырое яйцо становится крутым. Это явление называют денатурацией белка. Каждая хозяйка знает: чтобы приготовить вкусный бульон, надо нарезанное мясо положить в холодную воду. А когда хотят приготовить отварное мясо, то большие куски опускают в кипяток. Есть ли в этом химический смысл? Попробуем разобраться.
Налейте и пробирку холодной воды, опустите в нее немного сырого рубленого мяса и нагрейте. По мере нагревания образуются (и в большом количестве) серые хлопья. Это свернувшийся белок, пена, которую снимают шумовкой, чтобы не портила вид и вкус бульона. При дальнейшем нагревании растворимые в воде вещества постепенно переходят из мяса в раствор. Эти вещества называют экстрактивными, потому что они извлекаются из мяса при его экстракции кипящей водой (проще говоря, при варке бульона). Они-то, в первую очередь, и придают бульону характерный вкус. А мясо, лишившись этих веществ, становится менее вкусным.
В другой пробирке воду вскипятите заранее и положите сырое мясо уже в кипяток. Как только мясо соприкоснется с водой, оно моментально станет серым, зато хлопьев образуется очень мало. Тот белок, что находился на поверхности, под действием высокой температуры сразу свернулся и закупорил многочисленные поры, которые пронизывают мясо. Экстрактивные вещества, и белки в том числе, уже не могут перейти в раствор. Значит, они остаются внутри мяса, придавая ему хороший вкус и аромат. А бульон, разумеется, получается несколько хуже.
Белок денатурируется (свертывается) не только при нагревании. Налейте в пробирку чуть-чуть свежего молока и капните одну-две капли уксуса или раствора лимонной кислоты. Молоко тут же скиснет, образуя белые хлопья. Это свертывается молочный белок. Кстати, без такой реакции не приготовить творога, и не случайно творог так полезен - в него переходит почти весь молочный белок.
Когда молоко оставляют в теплом месте, то его белок тоже свертывается, но уже по иной причине- это работают молочнокислые бактерии. Их известно очень много, и все они вырабатывают молочную кислоту, даже если питаются не молоком, а, скажем, соком капусты. Профильтруйте немного скисшего молока и прибавьте к сыворотке несколько капель какого-нибудь самодельного индикатора. Цвет индикатора покажет, что в растворе есть кислота. Эта кислота - молочная, ее же можно обнаружить и в капустном, и в огуречном рассоле,
В состав некоторых белковых молекул входит, помимо углерода, водорода, кислорода и азота, еще и сера. В этом можно убедиться на опыте. Немного яичного белка поместите в пробирку с раствором едкого натра или стиральной соды и, нагрев пробирку, добавьте в нее немного раствора основного ацетата свинца Рb(СН 3 СОО) 2 * 3Н 2 O - свинцовой примочки, которая продается в аптеках. Если содержимое пробирки почернеет, значит, сера есть: это образуется сульфид свинца PbS, вещество черного цвета.
И в заключение приготовим настоящий белковый клей - казеиновый, которым пользуются по сей день, несмотря на обилие синтетических клеев. Казеин - это основа творога, а если так, то клей мы будем делать из молока, точнее, из его белковых веществ,
Отфильтруйте простоквашу от сыворотки. То, что осталось на фильтре, несколько раз промойте водой, чтобы удалить растворимые примеси, и высушите. Потом промойте полученную массу бензином и высушите вновь; это нужно для того, чтобы избавиться от молочного жира (он растворяется в бензине). Когда масса станет совсем сухой, измельчите ее в ступке - получится порошок казеина.
Сделать из него клей совсем просто - смешать порошок с нашатырным спиртом и водой в отношении 1:1:3. Конечно, вы захотите испытать клей. Попробуйте склеить им какие-нибудь деревянные или керамические предметы, потому что для этих материалов казеиновый клей особенно хорош.
О. Ольгин. "Опыты без взрывов"
М., "Химия", 1986
Цель работы: доказать присутствие в биологических объектах таких важных органических соединений, как белки, липиды, углеводы
Ход работы:
1 Определение глюкозы в виноградном соке
К 2 см3 виноградного сока добавьте 1 см3 раствора едкого натра и 3 капли раствора сульфата меди. Нагрейте до кипения.
Аналитический эффект: наблюдается образование желтого осадка Cu(OH)2, который при дальнейшем нагревании переходит в красный осадок Cu2О.
2 Реакция крахмала с йодом
К 2 мл раствора крахмала прибавляют 1–2 капли раствора Люголя. Раствор окрашивается в синий цвет. Затем нагревают. Окраска исчезает, но окраска вновь появляется при охлаждении.
3. Физико-химические свойства жиров
Взять 2 пробирки. В первую налить 2мл дистиллированной воды, во вторую – спирта. В каждую пробирку налить по 5 капель растительного масла. Все пробирки хорошо взболтать и отметить растворение жира в разных веществах.
4. Эмульгирование жиров
Взять 2 пробирки. В каждую из них налить по 3 мл дистиллированной воды и свежее растительное масло. Во вторую пробирку добавить несколько капель 10% раствора соды Na2CO3. Все пробирки закрывают, тщательно взбалтывают. Оставляют на 5 мин стоять и наблюдают стойкость эмульсии.
5. Определение непредельности жира
В пробирку внести 0,5-1г масла, прилить 2 капли КМnО4 и тщательно взболтать. Происходит обесцвечивание перманганата.
6. Биуретовая реакция на определение пептидной связи
В пробирку внести 5 капель 1%-ного раствора яичного белка, 3 капли 10-%- ного раствора NaOH и одну каплю 1%-ного раствора CuSO4 и перемешать. Содержимое пробирки приобретает сине-фиолетовое окрашивание.
7. Ксантопротеиновая реакция
К 5 каплям 1%-ного раствора яичного белка приливают 3 капли концентрированной азотной кислоты (осторожно!) и нагревают. Появится осадок желтого цвета. После охлаждения в пробирку добавьте 5-10 капель 10%-ного раствора NaOH до появления оранжевого окрашивания (оно связано с образованием натриевой соли этих нитросоединений).
8. Свертывание белков при нагревании
В пробирку нальем немного раствора белка. Нагреем раствор до кипения. Раствор мутнеет, белок выпадает в виде хлопьев. Свертывание белков при кипении - процесс необратимого осаждения, белковые молекулы меняют свою структуру.
9. Осаждение белков солями тяжелых металлов, спиртом, серной кислотой
В две пробирки приливаем раствор белка. В первую пробирку добавляют раствор сульфата меди (II), во вторую – раствор нитрата серебра. В обеих пробирках выпадают осадки. Соли тяжелых металлов осаждают белки из растворов, образуя с ними нерастворимые в воде солеобразные соединения.
К раствору белка прибавляем немного этилового спирта. Раствор мутнеет. При действии спирта происходит денатурация белка – разрушение его структуры.
К раствору белка прибавляем немного серной кислоты. Выпадает осадок. При действии серной кислоты происходит денатурация белка – разрушение его структуры.
Отчет по лабораторной работе оформите в виде таблицы (каждый опыт отдельно)
Исходные веществаЧто делали?Что наблюдали?Выводы, уравнения реакцииАльбумины
 Альбумины
Альбумины
 Действие на белок солей тяжёлых металлов
Действие на белок солей тяжёлых металлов



Существуют несколько несложных способов, как определить белок . Для этого воспользуемся некоторыми его характерными свойствами.
Одна из групп, на которые разделяются все существующие белки – это белки . Эта группа наиболее распространена и наиболее известна. К альбуминам относится белок из куриных яиц, содержится в крови человека и животных, а также в растениях, мышцах и молоке.
Чтобы определить эту группу белка, воспользуемся её свойствами растворимости в воде. Если альбумины нагревать – они изменяют свою структуру, то есть «сворачиваются».
Итак, попробуем определить белок . Используем, например, сыворотку коровьей крови или яичный сырой белок. Поместим его в кастрюльку, можно разбавить водой и буден нагревать на медленном огне до кипения. Растворим немного соли в белковом растворе и прильём немного Оцет (уксусную кислоту).
В результате реакции увидим, что из раствора будут выпадать белые хлопья.
Определить белок можно и другим простым способом: белок изменяют структуру под воздействием спирта, поэтому достаточно к белковому раствору прилить такой же объём спирта. Так же, как и в предыдущем случае, мы увидим выпадение белка в виде белых хлопьев.
А вот следующий интересный опыт можно назвать ещё и полезным. Определить белок можно, используя соли тяжёлых металлов. Например, соль меди, железа, свинца (медный купорос CuSO 4 , хлориды железа FeCl 2 , FeCl 3 , нитрат свинца Pb(NO 3) 4 и др.). Если к водному раствору белка добавить одну (или несколько) таких солей, то выпадает осадок химического соединения белка с тяжёлым металлом. Для нашего организма, да и для организма животных соли тяжёлых металлов – ядовитые вещества, способствующие разрушению белка!
Определить белок также можно с помощью действия не него минеральных кислот (кроме ортофосфорной H 3 PO 4). Если в пробирку налить азотную кислоту, а затем, осторожно, по стенке пробирки капнуть раствор белка, то по окружности стенки пробирки образуется белое кольцо выпавшего белка.
Ещё одна группа белков, называемая глобулинами – в отличии альбуминов не - растворяется в воде. Глобулины хорошо растворимы, если в растворе присутствуют соли. Содержатся глобулины в некоторых частях растений, молоке и мышцах живых организмов. К тому же установлено, что глобулины, выявленные в растениях, растворяются в 70% спирте!
И ещё одна группа белков – склеропротеины , к которым относятся ткани живых организмов, например, ногти, волосы, роговица глаза, а также костные ткани, рога животных и шерсть. Склеропротеины не растворяются в воде и не растворяются в спирте, но при их обработке сильными растворами кислот они приобретают способность растворяться, при этом частично разлагаться.
Глобулины
и склеропротеины
можно определить с помощью ксантопротеиновой реакции
. Это цветная реакция определения белка, при которой, если нагреть пробу, содержащую белок, то проба изменит цвет на жёлтый. Затем при нейтрализации кислоты щёлочью цвет поменяется на оранжевый.
Такую реакцию, возможно, некоторым уже приходилось наблюдать на собственном опыте, когда на кожу попадала азотная кислота.
Следующая реакция по определению белка - биуретовая , которая заключается в добавлении разбавленного раствора натриевой или калиевой щёлочи к раствору белка. В тот же раствор необходимо добавить несколько капель раствора медного купороса. Наблюдаем изменение цвета раствора на красный, затем фиолетовый и сине-фиолетовый.
Если белок длительно нагревать в растворе кислот, то он будет расщепляться на составляющие – пептиды, затем до составляющих его аминокислот, что применяют в промышленности для приготовления приправ к пище.
Урок — практическая работа
Тема «Анализ качества пищевых продуктов. Обнаружение белка в исследуемой пробе».
подготовила учитель химии МАОУ лицея №28 имени Н.А.Рябова
Попова С.И.
Цель: «Определить качество пищевых продуктов. Исследовать предложенные пробы на содержание белка».
Задачи:
1.Образовательные:
формировать умения решать экспериментальные задачи прикладного характера на установление содержания белков в пищевых продуктах;
установить межпредметные связи изучаемой теоретической основы с близкими, «домашними» проблемами.
2.Воспитательные:
продолжить формирование ответственного, творческого отношения к выполнению заданий, точность, наблюдательность, настойчивость;
продолжить краеведческое воспитание;
воспитание позитивного отношения к ЗОЖ; воспитание толерантности, сотрудничества, самостоятельности.
3.Развивающие:
развивать умения переносить знания в новые условия;
развивать умение проводить, наблюдать и описывать химический эксперимент;
развивать мыслительные операции (анализ, синтез, установление причинно — следственных связей, выдвижение гипотезы, классификация, проведение аналогий, обобщение, умение доказывать, выделение главного);
совершенствовать коммуникативные умения учащихся в совместной деятельности (умение вести диалог, выслушивать оппонента, аргументировано обосновывать свою точку зрения).
Умения:
1. Общелабораторные – проводить нагревание; фильтрование.
2. Организационные — соблюдать аккуратность и чёткость в работе, ПТБ, работать по инструкции, поддерживать чистоту рабочего места, оформлять записи, осуществлять самоконтроль.
(вступительное слово учителя)
Белки в продуктах питания играют роль главного строительного материала для организма, без которого невозможна его жизнедеятельность, рост и восстановление клеток.
Как вы наверняка уже знаете, любой продукт состоит из белков, жиров и углеводов, и основной нашей задачей является умелое их сочетание в нашем ежедневном рационе.
Один из главных принципов здорового питания как раз и говорит о том, что пища должна быть сбалансированной, и содержать оптимальное количество белков, жиров и углеводов.
Белковая пища – один из важнейших компонентов рациона любого человека. При недостатке белков невозможен процесс расщепления жиров, в свою очередь сытный белковый продукт позволяет увеличить время усвоения углеводов, помогая поддерживать стабильный уровень сахара в крови и подавляя чувство голода.
А какое строение имеет белок? (Работа с комплексом «Наглядна я школа»-структуры белка)
Качественные реакции на белок обсудить
(Переход к новой теме)
Оценка качества пищевых продуктов, определение микробиологической зараженности – очень ответственные и трудоемкие процессы. Подход к каждому образцу производится строго индивидуально.
Существует несколько типов исследования качества пищевой продукции:
органолептическое – запах, вкус, цвет, мутность, температура, посторонние пленки, осадки;
физико-химическое – качественный состав заявленной пробы, наличие примесей (как физических, так и химических);
микробиологическое – определение наличия в исследуемой пробе посторонних микроорганизмов, инфекций (особенно важный тип исследований, рекомендованный Analytic Company для детского питания);
комплексное – экспертиза на соответствие продукта определенном ГОСТ, ГОСТ Р, ТУ, СаНПин и другим нормам, устанавливающим критерии безопасности для человека.
Ребята делятся на 4 группы и проводят по 2 опыта по предварительно выданной инструкции . Затем все ученики заполняют лабораторный журнал с последующим обсуждением результатов.
ПЕРЕД выполенением практики повторить правила техники безопасности !
Опыт №1.Определение качества пастеризации молока.
Пастеризацией предусматривается уничтожение патогенных микроорганизмов, которые ухудшают качество молока. Содержание белка при этом не должно уменьшаться.
1.К 3 мл молока добавить 3 мл дистиллированной воды.
2.По каплям добавлять 0.1 Н раствор H 2 SO 4 хлопьев казеина. Отфильтровать.
3. Фильтрат. Нагреть до кипения.
КЛЮЧ. В сыром молоке вновь появляются хлопья казеина .
4.Предположите степень пастеризации молока в исследуемых пробах.
5.Предположите причины фальсификации различных проб.
6. К полученной пробе добавьте несколько капель концентрированной азотной кислоты. Нагрейте. Желтое окрашивание свидельствует о наличии в белке ароматических колец.(ксантопротеиновая реакция).
Опыт №2.
Определение свежести молока
К 3 мл 1% раствора фенола прилить 3 мл 1% раствора хлорида железа (III ), отметить фиолетовое окрашивание, добавить 3 мл молока.
КЛЮЧ. Скисшее молоко дает желто-зеленое окрашивание.
Установите степень свежести, причины фальсификации разных проб.
Опыт №3.
Определение примеси в сметане.
В химический стакан налить 10 мл горячей воды. В горячую воду поместить ложечку сметаны.
КЛЮЧ. При наличии примеси (творога, кефира, крахмала) жир всплывет, а казеин осядет на дно.
Зная, что в норме сметана не должна иметь осадка, предположите причины фальсификации разных проб.
Опыт №4
Определение свежести мяса.
1. Приготовить мясной бульон. (4 мл воды+кусочек мяса до кипения нагреть).
2. Отфильтровать в колбу, пользуясь воронкой.
3.Добавить 5 капель % H 2 SO 4 и через несколько минут отметить результат.
КЛЮЧ. В свежем бульоне раствор прозрачный, при сомнительной свежести раствор становится мутным, а у безусловно несвежего мяса желеобразный осадок с хлопьями.
Определите степень фальсификации пробы. Сравните несколько разных проб. Предположите причины различных результатов.
Опыт №5.
Определение белка в предложенных продуктах.
1В 3 пробирки налить 4 мл воды. В 1 добавить 0,5 бульонного кубика, во 2-ю кусочек мяса, в 3-ю кусочек сосиски. Прокипятить.
2.Отфильтровать.
3.В каждую пробирку добавить концентрированную HNO 3 по каплям и немного нагреть.
КЛЮЧ. В растворе, в котором присутствует белок будет желтое окрашивание.
Сделать вывод о качестве проб.