Inclus dans tous les produits alimentaires. En termes de volume qu'elle occupe dans la masse totale de nombreux produits alimentaires, l'eau est le composant le plus important et elle affecte bon nombre de leurs caractéristiques qualitatives, notamment leur consistance et leur structure. La teneur en eau la plus élevée est typique des fruits et légumes (72-95%), du lait (87-90%), de la viande (58-74%), du poisson (62-84%). On trouve beaucoup moins d'eau dans la margarine, le beurre (15,7-32,6 %), l'amidon (14-20 %), les céréales, la farine, les céréales, les pâtes, les fruits secs, les légumes et les champignons, les noix (10-14 %), le thé (8,5 %). La quantité minimale d'eau est contenue dans le lait en poudre (4,0%), le caramel au caramel (3,6%), le sel de table (3,0%), les graisses de cuisson (0,3%), l'huile végétale et le sucre (0,1%).
Dans les tissus animaux et végétaux, l’eau est le composant le plus variable de la composition chimique. Par exemple, dans les pommes de terre, selon la variété économique et botanique, la zone de culture, le sol, les conditions climatiques et la saison de croissance, la quantité d'eau varie de 67 à 83 %.
Dans les produits fabriqués à partir de matières premières végétales et animales – sucre, confiseries, fromages… – la teneur en eau est réglementée par des normes.
Pour de nombreux aliments, la teneur en eau (humidité) est un indicateur de qualité important. Une teneur en eau réduite ou augmentée par rapport à la norme établie pour le produit entraîne une détérioration de sa qualité. Par exemple, une diminution de l'humidité dans la marmelade et la confiture aggrave leur consistance et leur goût ; la perte d'humidité dans les fruits et légumes frais réduit la turgescence cellulaire de 5 à 7 %, de sorte qu'ils deviennent lents, flasques, leur qualité diminue fortement et ils se détériorent rapidement.
Les produits à forte teneur en eau sont instables pendant le stockage, car des micro-organismes s'y développent rapidement. L’eau contribue à accélérer les processus chimiques, biochimiques et autres dans les produits alimentaires. La viande et le poisson crus sont facilement affectés par les bactéries, et les fruits et légumes sont facilement affectés par les moisissures.
Les produits à faible teneur en eau se conservent mieux ; la farine, les céréales, les pâtes, les fruits et légumes secs et autres produits se conservent longtemps ; à forte humidité, ces produits moisissent rapidement pendant le stockage.
Cependant, différents aliments ayant la même teneur en humidité sont souvent stockés différemment. Il a été constaté qu'il est important de savoir quelles formes de liaison l'eau est liée aux principales substances des produits alimentaires. Pour prendre en compte ces facteurs, au début des années 50 du siècle dernier, un nouveau concept est apparu : activité d'eau, désigné par le signe a w. L'activité de l'eau a w est exprimée par le rapport de la pression de vapeur de l'eau au-dessus d'un produit donné à la pression de vapeur de l'eau au-dessus de l'eau pure à la même température. L'activité de l'eau caractérise l'état de l'eau dans les produits alimentaires et détermine sa disponibilité pour les réactions chimiques, physiques et biologiques. Généralement, plus l’eau est dans un état lié, moins elle est active. Mais même l’eau liée, sous certaines conditions, peut avoir une certaine activité.
En fonction de l'activité de l'eau, les produits alimentaires sont divisés en trois groupes :
1. Produits alimentaires frais riches en eau, dans lesquels son activité est de 0,95 à 1,0. Il s’agit notamment des légumes frais, des fruits, des jus de fruits, du lait, de la viande, du poisson, etc. ;
2. Produits alimentaires transformés avec une activité de l'eau de 0,90 à 0,95. Il s'agit notamment du pain, des saucisses bouillies, du jambon, du fromage cottage, etc. ;
3. Produits alimentaires avec une activité de l'eau jusqu'à 0,90. Ceux-ci comprennent le fromage, le beurre, les saucisses fumées, les fruits et légumes secs, les céréales, la farine, la confiture, etc. L'activité de l'eau dans ces produits est généralement de 0,65 à 0,85 et la teneur en humidité est de 15 à 30 %.
Pour éviter un certain nombre de réactions physicochimiques et biochimiques qui réduisent la qualité des produits alimentaires lors du stockage et leur altération microbiologique, un moyen efficace consiste à réduire l'activité de l'eau dans les produits alimentaires. Pour ce faire, on utilise le séchage, le séchage, l'ajout de diverses substances (sel, sucre, etc.) et la congélation. La faible activité de l'eau inhibe le développement de micro-organismes et les réactions physico-chimiques et biochimiques. Pour chaque type de micro-organisme, il existe un seuil inférieur d'activité de l'eau, en dessous duquel leur développement s'arrête.
En plus d’influencer les processus qui se produisent pendant le stockage des aliments, l’activité de l’eau est également importante pour la texture des aliments. L'activité maximale de l'eau autorisée dans les produits secs sans perte des propriétés souhaitées est de 0,34 à 0,50, selon le produit (lait en poudre, craquelins). Une activité élevée de l’eau est nécessaire pour les produits à texture douce qui ne doivent pas être cassants.
Les produits alimentaires sont hygroscopiques . L'hygroscopique fait référence à la capacité des produits à absorber et à retenir la vapeur d'eau de l'atmosphère environnante. L'hygroscopique dépend des propriétés physiques et chimiques des produits, de leur structure, de la présence de substances retenant l'eau, ainsi que de la température, de l'humidité et de la pression de l'air ambiant. .
Lors du stockage des produits alimentaires, une teneur en humidité d'équilibre est créée, dans laquelle l'humidité n'est pas absorbée par les produits de l'environnement et l'humidité ne passe pas des produits dans l'environnement. Cet état se produit lorsque la pression de vapeur d'eau au-dessus des produits est égale à la pression partielle de vapeur d'eau dans l'espace environnant à la même température de l'air ambiant et du produit.
La teneur en humidité d'équilibre des produits est de nature dynamique, car elle change en fonction des conditions extérieures - humidité, température et pression de l'air, ainsi que des propriétés physiques et chimiques du produit. Lorsque les conditions extérieures changent, la teneur en humidité d'équilibre des produits change puis se rétablit à un nouveau niveau.
Lors du choix des conditions de stockage des produits alimentaires, il est recommandé de créer une humidité relative de l'air à laquelle les produits ne sont pas gâtés par des micro-organismes et ne réduisent pas leur qualité en raison du dessèchement, du flétrissement ou d'une humidité excessive. Ainsi, lors du stockage de la farine, l'humidité relative de l'air doit être de 70 %, les pommes de terre et pommes fraîches de 90 à 95, les légumes verts de 100 %.
L'eau est incluse dans tous les produits alimentaires. La teneur en eau la plus élevée est typique des fruits et légumes (72-95%), du lait (87-90%), de la viande (58-74%), du poisson (62-84%). On trouve beaucoup moins d'eau dans les céréales, la farine, les céréales, les pâtes, les légumes et fruits secs, les noix, la margarine et le beurre (12-25 %). La quantité minimale d'eau est contenue dans le sucre (0,14-0,4 %), le beurre végétal et le beurre clarifié, les graisses de cuisson (0,25-1,0 %), le sel de table, le thé, le caramel sans garniture, le lait en poudre (0,5 -5 %).
| Le contenu de l'article : |
L'eau dans les produits naturels
Dans les produits naturels, l’eau est le composant le plus mobile de la composition chimique des tissus. Ainsi, la teneur en eau du hareng frais varie dans une large gamme - de 51,0 à 78,3 %, chez la morue - de 70,6 à 86,2 %, selon l'âge, le sexe, la zone et l'heure de pêche. La quantité d'eau dans les pommes de terre peut être comprise entre 67 et 83 %, dans les melons entre 81 et 93 % et dépend de la variété économique et botanique des légumes, de la zone de leur culture et de la météo de la saison de croissance.
Dans les produits fabriqués à partir de matières premières végétales et animales - sucre, confiseries, charcuteries, fromages et autres - la teneur en eau est réglementée par des normes.
Les fonctions normales du corps des animaux et des plantes ne sont réalisées qu'avec une teneur en eau suffisante dans les tissus. Les fruits et légumes présentant une perte d'eau de 5 à 7 % se fanent et perdent leur fraîcheur.
La perte d'eau des animaux dans une proportion de 15 à 20 % entraîne leur mort. Il est impliqué dans de nombreuses réactions biochimiques au cours de la vie de l'organisme et dans des changements biochimiques post-mortem. L'eau est nécessaire aux processus chimiques et colloïdaux qui se produisent dans les tissus animaux et végétaux lors de leur transformation.
Le corps adulte contient 58 à 67 % d’eau. En moyenne, une personne consomme environ 40 g d'eau par kilogramme de poids corporel et par jour, et elle perd la même quantité sous forme d'excrétions diverses. Une personne peut exister sans nourriture pendant environ un mois, tandis que sans eau - pas plus de 10 jours.
Une personne reçoit une partie de la quantité d'eau requise (environ 50 %) grâce à la nourriture, l'autre partie grâce à la consommation de boissons et d'eau potable. 350 à 450 g d'eau sont formés chaque jour dans le corps humain au cours des processus oxydatifs (l'oxydation de 1 g de graisse produit 1,07 g d'eau, 1 g d'amidon - 0,55 g et 1 g de protéines - 0,41 g d'eau).
Les propriétés des produits dépendent non seulement de la quantité d'eau qu'ils contiennent, mais également de la forme de leur liaison avec d'autres substances.
L'eau, qui fait partie des produits alimentaires, présente trois formes de communication avec les substances sèches : physico-mécanique (humidité mouillante, humidité dans les macro et microcapillaires), physico-chimique (gonflement de l'humidité, adsorption) et chimique (liaisons ioniques et moléculaires). ). Les deux premières formes de collage prédominent ; le collage chimique est rare dans les produits.
Mouillage par l'humidité
L'humidité mouillante est de l'humidité sous forme de minuscules gouttelettes à la surface des produits ou sur la surface coupée des tissus alimentaires. Il est maintenu en place par les forces de tension superficielle.
Humidité macro et microcapillaire
L'humidité macrocapillaire est l'humidité située dans les capillaires d'un rayon supérieur à 10 à 5 cm, l'humidité microcapillaire dans les capillaires d'un rayon inférieur à 10 à 5 cm. L'humidité macro et microcapillaire est une solution contenant des substances minérales et organiques du produit. . Il est retenu par la force de capillarité dans les interstices du système capillaire structurel des produits.
Lors de la découpe de viande, de poisson, de fruits et de légumes sous action mécanique, une perte partielle de l'humidité capillaire structurelle sous forme de jus de muscle, de fruit et de légume, qui ont une haute valeur nutritionnelle, peut se produire.
L'humidité mouillante est plus facilement éliminée du produit et elle est moins étroitement liée au support. L'humidité capillaire est associée mécaniquement et en quantité indéfinie aux substances sèches du produit. L’humidité microcapillaire est plus difficile à éliminer d’un produit que l’humidité macrocapillaire.
Gonflement dû à l'humidité
L'humidité gonflée, également appelée humidité retenue osmotiquement, se trouve dans les microespaces formés par les membranes cellulaires, les molécules de protéines fibrillaires et d'autres structures fibreuses. Il est maintenu en place par les forces osmotiques.
L'humidité retenue de manière osmotique se trouve dans le jus des cellules, déterminant leur turgescence et influençant les propriétés plastiques des tissus animaux. L'humidité gonflante est faiblement liée aux substances sèches du produit et est éliminée pendant le séchage plus tôt que l'humidité microcapillaire.
L'humidité mouillante, micro-, macrocapillaire et osmotique, est appelée eau libre des produits alimentaires. L'eau libre possède les propriétés physiques et chimiques habituelles : sa densité est de l'ordre de l'unité, son point de congélation est d'environ 0°, elle s'élimine lors du séchage et de la congélation des produits et c'est un solvant actif. Grâce à cela, il se produit principalement une perte de poids naturelle - un rétrécissement des produits pendant le stockage et le transport.
Eau liée à l'adsorption
L'eau liée à l'adsorption se situe à l'interface entre les particules colloïdales et l'environnement. Il est fermement retenu par un champ de force moléculaire et fait partie des micelles de divers colloïdes hydrophiles, parmi lesquels les protéines hydrosolubles sont les plus importantes. Par conséquent, ce type d’humidité est appelé eau liée ou eau d’hydratation.
Il ne dissout pas les substances organiques et les sels minéraux, gèle à basse température (-71°), a une faible constante diélectrique et n'est pas absorbé par les micro-organismes.
Les graines de plantes et les spores de micro-organismes tolèrent les basses températures, car l'eau qu'elles contiennent est hydratante et ne forme pas de cristaux de glace susceptibles d'endommager les cellules des tissus.
L'eau liée avec une forme chimique de liaison comprend l'humidité de cristallisation, qui entre dans la composition des molécules en quantité strictement définie, par exemple dans la composition du sucre du lait (C12H22O11 HgO), du glucose (C6H12O6 H2O). Il est éliminé par calcination de composés chimiques, entraînant la destruction du matériau.
Il n’y a pas de frontière nette entre l’eau liée et l’eau libre des produits. Les molécules d'eau sont polaires (les charges électriques sont situées asymétriquement dans une molécule d'eau : son extrémité oxygène porte une charge négative et son extrémité hydrogène porte une charge positive), donc les molécules d'eau qui sont orientées en fonction du signe et de l'ampleur de la charge de les particules colloïdales sont les plus étroitement liées.
Les molécules situées plus près de la micelle sont retenues plus fermement par les forces d’attraction électrostatiques. Plus les molécules d’eau sont éloignées de la particule colloïdale, plus la liaison est faible. Les molécules d'eau de la couche la plus externe sont moins associées aux micelles et peuvent échanger avec des molécules d'eau libres.
L'eau libre prédomine dans les tissus végétaux et animaux. Ainsi, dans les muscles des animaux et des poissons, la majeure partie de l'eau est associée à des protéines hydrophiles dues aux forces osmotiques (45-55 %), capillaires (40-45 %), à l'eau mouillante (0,8-2,5 %) et la part de l'eau liée ne représente que 6,5 à 7,5 %. - Jusqu'à 95 % de l'eau libre se trouve dans les fruits et légumes. Par conséquent, ces produits sont séchés jusqu'à une teneur en humidité résiduelle de 8 à 20 %, car l'eau libre en est facilement éliminée.
L'eau présente dans les produits alimentaires pendant la transformation et le stockage peut passer de libre à liée, et vice versa, ce qui entraîne une modification des propriétés des produits. Par exemple, lors de la cuisson du pain, de la cuisson des pommes de terre, de la production de marmelade, de guimauves, de gelées et de gelées, une partie de l'eau libre est convertie en adsorption associée aux particules colloïdales de protéines, d'amidon et d'autres substances, et la quantité d'humidité retenue osmotiquement augmente également.
Dans les jus de fruits, de baies et de légumes, les formes des liaisons aqueuses changent par rapport aux matières premières d'origine. Lorsque le pain rassis et que la marmelade est trempée, à cause du vieillissement des gelées, lorsque la viande congelée et les pommes de terre décongèlent, on observe une transition d'une partie de l'eau liée en eau libre.
Produits alimentaires pendant le stockage et le transport
Lors du stockage et du transport, les produits alimentaires absorbent ou libèrent de la vapeur d'eau de l'extérieur, selon les conditions. Dans le même temps, leur masse augmente ou diminue. La capacité des produits à absorber et à libérer de la vapeur d’eau est appelée hygroscopique. La quantité d'eau qu'un produit absorbe ou libère dépend de l'humidité, de la température et de la pression de l'air ambiant, de la composition chimique et des propriétés physiques du produit lui-même, ainsi que de l'état de sa surface, du type et de la méthode d'emballage.
L'hygroscopique la plus élevée se trouve dans le lait en poudre, la poudre d'œuf, les fruits et légumes secs, l'amidon, etc. L'humidité absorbée de l'air, appelée hygroscopique, peut être trouvée dans un produit à l'état libre ou lié.
Les conditions et périodes de stockage d'un certain nombre de produits dépendent du rapport entre l'eau libre et l'eau liée qu'ils contiennent. Par exemple, les céréales, la farine et les céréales sont bien conservées à une humidité allant jusqu'à 14 %, car presque toute leur humidité est à l'état lié. À mesure que leur teneur en eau augmente, l'humidité libre s'accumule également, les processus biochimiques s'intensifient et des difficultés de stockage surviennent donc.
Les produits à forte teneur en eau libre (viande, poisson, lait, etc.) se conservent mal et sont périssables. Pour un stockage à long terme, ils sont en conserve.
Humidité du produit
La teneur en humidité d'un produit est le rapport entre l'eau libre et liée à l'adsorption et sa masse d'origine, exprimé en pourcentage.
Pour de nombreux aliments, la teneur en eau (humidité) est un indicateur de qualité important. Une teneur en eau réduite ou augmentée par rapport à la norme établie pour le produit entraîne une détérioration de sa qualité. Par exemple, la farine, les céréales et les pâtes très humides moisissent rapidement pendant le stockage, et une diminution de l'humidité de la marmelade et de la confiture aggrave leur consistance et leur goût.
La perte d'humidité des fruits et légumes frais réduit la turgescence cellulaire, de sorte qu'ils deviennent léthargiques, flasques et se détériorent rapidement.
Notre expert dit - nutritionniste, candidat en sciences médicales Ivan Demidov.
La soif est tout !
Dans le corps humain, qui est composé à près de 90 % d’eau, ce fluide est d’une importance primordiale. Son absence peut entraîner de graves problèmes de santé. Mais en ajoutant simplement de l'eau à votre alimentation, vous pouvez perdre du poids et améliorer votre bien-être.
Notre corps subit une déshydratation particulièrement sévère le matin. Après tout, la nuit, jusqu'à 500 ml d'humidité en sortent. Alors, comment la plupart d’entre nous peuvent-ils combler ce déficit ? Le matin, nous nous réveillons et nous nous asseyons pour prendre le petit-déjeuner. Nous sommes toujours détendus, mais le corps a déjà commencé à travailler activement : il a besoin de libérer de l'humidité pour humidifier les aliments avec de la salive, et il faut encore un peu d'eau pour lubrifier l'œsophage, produire du suc gastrique et aussi pour protéger l'estomac des agents agressifs. action de l'acide chlorhydrique.
Tout comme le tube digestif, les cellules du cerveau ont également besoin d’eau. Mais où le trouver ? Pas dans une petite tasse de café, à laquelle la plupart d’entre nous se limitent le matin ? Le corps n'a d'autre choix que de puiser l'eau dont il a besoin dans les cellules (jusqu'à 66 %) et dans l'espace intercellulaire (jusqu'à 26 %). Un corps déshydraté peut réagir à une telle attaque par une augmentation de l’acidité, de la goutte et des calculs rénaux.
L'emprunt d'eau du sang (jusqu'à 8 %) entraîne des troubles circulatoires, une augmentation de la pression artérielle et des capillaires obstrués - à l'origine d'accidents vasculaires cérébraux et de crises cardiaques. La soif interne chronique peut aussi parfois s'exprimer sous forme de nausées, de migraines, de douleurs articulaires, de constipation, et une carence en H2O fait vieillir la peau, entraîne l'apparition de rides prématurées, d'acné, de cellulite et même une prise de poids - le fait est que le corps En cas de manque d'humidité, il faut garder de l'eau en réserve dans les plis adipeux (un peu comme un chameau la stocke dans ses bosses).
Boire ou ne pas boire?
En moyenne, nous avons besoin de 1,5 à 2,5 litres d'eau par jour (le ratio moyen est le suivant : pour 1000 kilocalories consommées, nous avons besoin d'environ 1 litre d'eau). Certes, nous obtenons environ 60 % de l’humidité nécessaire grâce aux aliments.
Notre propre corps peut nous dire si nous avons suffisamment d'H2O ou non : pour ce faire, nous devons faire attention à la couleur de notre urine. S’il fait sombre, cela signifie que la personne ne boit pas suffisamment et doit augmenter sa consommation de liquide. Deuxième test : pincez votre main à l’extérieur de votre paume. Si la peau se lisse rapidement, tout va bien ; si elle se lisse lentement, les cellules ont besoin d'humidité.
Il y a des gens qui essaient, au cas où, de dépasser le plan d'approvisionnement en H2O du corps. Cependant, un excès de cette substance ne vaut pas mieux qu’un manque. Trop d'eau entraîne le lessivage des minéraux (potassium, calcium, sodium) du corps, brouille partiellement la microflore intestinale, perturbe l'absorption des nutriments et des vitamines, augmente la pression intracrânienne et artérielle, provoque des convulsions, des gonflements et même des crises cardiaques.
La consommation d'eau est particulièrement dangereuse pour les personnes souffrant d'insuffisance rénale et d'hypertension. Ils devraient limiter la quantité de liquide à 1,5 litre par jour. et il vaut mieux lutter contre la soif par d'autres moyens : manger plus de légumes et de fruits, prendre une douche fraîche dans la chaleur et boire du thé acidifié au citron, et aussi éviter les cornichons et les aliments fumés.
Il ne faut pas trop boire en faisant du sport. L'excès d'eau surcharge le système cardiovasculaire, qui travaille déjà très intensément sous l'influence de l'activité physique. Mais en même temps, vous ne pouvez pas faire d'exercice « à sec » - il est nécessaire de reconstituer la perte de liquide et de minéraux qui s'échappent par la sueur. Par conséquent, vous devez boire, mais pas beaucoup - quelques gorgées, et il vaut mieux ne pas utiliser d'eau minérale (elle assèche la bouche), mais de l'eau ordinaire. Il est bon de boire de l’eau minérale après le sport pour rétablir l’équilibre des fluides et des minéraux.
Les personnes qui souhaitent conserver une silhouette élancée ne devraient pas en faire trop. Le fait est que l'abondance de liquide étire l'estomac et qu'il commence à avoir besoin de plus de nourriture, c'est pourquoi une personne grossit naturellement. La règle est donc la suivante : buvez exactement autant que vous buvez facilement et avec plaisir. Et pas d'un seul coup, mais petit à petit, mais le plus souvent possible.
Que verser dans un verre ?
Tous les liquides ne sont pas bons pour le corps. Le thé, le café, les sodas et l'alcool contiennent bien sûr aussi de l'eau, mais ils contiennent aussi des substances déshydratantes comme la caféine, l'alcool, etc. Ces composants éliminent non seulement l'humidité contenue dans la boisson, mais emportent également avec eux des réserves d'eau, stocké dans le corps. Cela peut être clairement constaté en mesurant le volume d'urine qui sort après avoir bu de telles boissons. Vous verrez que la quantité de liquide quittant le corps sera bien supérieure à celle qui y est entrée. N'oubliez pas de déduire également le coût de la transpiration, à l'aide de laquelle le corps refroidit le corps enflammé par les boissons fortes.
Il est donc préférable de boire de l’eau pure et plate. Vous pouvez utiliser des minéraux fondus ou filtrés régulièrement, ou des minéraux de table (minéralisation – 1 à 2 g/l ou moins). Vous pouvez boire cette eau à tout moment, en n’importe quelle quantité. Les eaux ayant une minéralisation de 8 à 12 g/l sont dites médicinales. Ce ne sont pas des boissons, mais des médicaments, ils doivent donc être utilisés uniquement sur prescription d'un médecin. Les eaux médicinales comprennent les eaux présentant une minéralisation de 2 à 8 g/l. Ces eaux sont utilisées aussi bien sur prescription médicale que comme boisson habituelle, mais pas systématiquement.
Excès de poids, lavez-vous !
Comment l’eau plate vous aide-t-elle à perdre du poids ? Premièrement, il contient 0 calorie, et en même temps, comme l'ont montré des études, boire 2 litres d'eau par jour entraîne une dépense énergétique dans l'organisme d'environ 400 kJ. Deuxièmement, l’eau améliore la digestion et nettoie l’organisme des toxines, dont 2 à 4 kg peuvent s’accumuler dans le tube digestif. Troisièmement : le liquide aide à traiter les graisses et les protéines et normalise généralement le métabolisme.
Et enfin, c’est l’eau qui nous aide à distinguer la sensation de faim et de soif. Il s’avère que très souvent nous les confondons. Tester votre appétit est simple : il vous suffit de boire un verre de liquide. Habituellement, environ 10 minutes plus tard, l’envie de manger disparaît, car le corps ne demandait qu’à boire.
Le régime de consommation habituel est de 2 à 2,5 litres d’eau par jour. Mais pour perdre du poids, il faut augmenter la quantité de liquide. Pour chaque kilogramme de poids corporel, il devrait y avoir 30 à 40 ml d’eau. Par conséquent, si vous pesez 80 kg, vous devez boire environ 3 à 3,2 litres par jour. Il est préférable de s'asseoir « sur l'eau » en été, lorsqu'une partie du liquide est perdue avec la sueur et que les reins et la vessie sont donc moins surchargés. De plus, si vous faites cela en hiver, l’excès de liquide dans le corps vous donnera une sensation de froid intense. Cependant, avant d'essayer un régime hydrique, vous devez consulter votre médecin et savoir si votre cœur, vos reins et votre tractus gastro-intestinal peuvent supporter une telle charge.
D'ailleurs
Le corps éprouve une soif particulièrement forte :
>> Pendant une activité physique.
>> Dans la chaleur ou dans les bains publics.
>> Pendant un voyage en avion (l'air dans la cabine de l'avion est très sec).
>> Pour les rhumes et toutes les maladies accompagnées d'une forte fièvre.
>> Lors de la prise de médicaments (beaucoup d'entre eux entraînent une déshydratation).
>> En fumant et en buvant des boissons et de l'alcool contenant de la caféine.
Dans toutes ces situations, il faut boire davantage sans attendre que la soif s’installe.
L’humidité nécessaire à l’organisme se trouve dans presque tous les aliments, notamment dans les légumes et les fruits.
|
Des produits |
|
|
Fruits frais |
79–90 |
|
Légumes verts |
|
|
Viande et poisson |
65–70 |
|
Lait |
|
|
Fromage blanc |
75–85 |
|
Pomme de terre |
|
|
Pain |
Introduction 2
Humidité libre et liée dans les produits alimentaires 3
Activité d'eau. Isothermes de sorption 9
Activité de l’eau et stabilité des aliments 13
Le rôle de la glace pour assurer la stabilité des aliments 17
Méthodes de détermination de l'humidité dans les produits alimentaires 19
Conclusion 20
Références 21
Introduction
L'eau est un composant important des produits alimentaires. Il est présent dans une variété de produits végétaux et animaux en tant que composant cellulaire et extracellulaire, en tant que milieu dispersant et solvant, déterminant leur consistance et leur structure et influençant l'apparence, le goût et la stabilité du produit pendant le stockage. Par son interaction physique avec les protéines, les polysaccharides, les lipides et les sels, l’eau contribue de manière significative à la texture des aliments.
La quantité d'eau présente dans les produits alimentaires affecte leur qualité et leur durée de conservation. Les aliments périssables à forte teneur en humidité ne peuvent pas être conservés longtemps sans mise en conserve. L'eau contenue dans les produits contribue à accélérer les processus chimiques, biochimiques et autres. Les produits à faible teneur en eau sont mieux conservés.
De nombreux types d’aliments contiennent de grandes quantités d’humidité, ce qui affecte négativement leur stabilité pendant le stockage. Étant donné que l'eau est directement impliquée dans les processus hydrolytiques, son élimination ou sa liaison en augmentant la teneur en sel ou en sucre inhibe de nombreuses réactions et inhibe la croissance des micro-organismes, prolongeant ainsi la durée de conservation des produits. Il est également important de noter que l’élimination de l’humidité par séchage ou congélation affecte considérablement la composition chimique et les propriétés naturelles.
L'objectif de ce travail est d'étudier les propriétés et le comportement de l'eau et de la glace dans les produits alimentaires.
Pour atteindre cet objectif, les tâches principales suivantes sont résolues :
Etude des différentes formes de raccordement à l'eau dans les produits alimentaires ;
Clarification de la relation entre l'activité de l'eau des produits alimentaires et leurs propriétés physico-chimiques, rhéologiques et technologiques, ainsi que les changements qualitatifs lors de la transformation et du stockage.
Humidité libre et liée dans les produits alimentaires
L'eau dans les produits alimentaires joue, comme déjà indiqué, un rôle important, puisqu'elle détermine la consistance et la structure du produit, et son interaction avec les composants présents détermine la stabilité du produit pendant le stockage.
La teneur totale en humidité d'un produit indique la quantité d'humidité qu'il contient, mais ne caractérise pas son implication dans les modifications chimiques, biochimiques et microbiologiques du produit. Pour assurer sa stabilité pendant le stockage, le rapport entre l'humidité libre et l'humidité liée joue un rôle important. L'humidité liée est de l'eau associée, étroitement liée à divers composants - protéines, lipides et glucides en raison de liaisons chimiques et physiques. L'humidité libre est l'humidité qui n'est pas liée par un polymère et qui est disponible pour les réactions biochimiques, chimiques et microbiologiques. Regardons quelques exemples.
Lorsque la teneur en humidité du grain est de 15 à 20 %, l'eau liée est de 10 à 15 %. Avec une humidité plus élevée, de l'humidité libre apparaît, ce qui améliore les processus biochimiques (par exemple, la germination des grains).
Les fruits et légumes ont une teneur en humidité de 75 à 95 %. Il s'agit principalement d'eau libre, mais environ 5 % de l'humidité est retenue par les colloïdes cellulaires dans un état étroitement lié. Par conséquent, les légumes et les fruits peuvent être facilement séchés à 10 - 12 %, mais le séchage à une humidité plus faible nécessite l'utilisation de méthodes spéciales.
La majeure partie de l'eau contenue dans le produit peut être transformée en glace à -5°C, et la totalité - à -50°C et moins. Cependant, une certaine proportion d’humidité étroitement liée ne gèle pas même à une température de -60°C.
« Liaison de l'eau » et « hydratation » sont des définitions qui caractérisent la capacité de l'eau à s'associer à différents degrés de force avec des substances hydrophiles. La taille et la force de la liaison de l'eau ou de l'hydratation dépendent de facteurs tels que la nature du composant non aqueux, la composition du sel, le pH et la température.
Dans un certain nombre de cas, le terme « eau liée » est utilisé sans préciser sa signification, mais un grand nombre de ses définitions sont proposées. Selon eux, l'humidité liée :
Caractérise la teneur en humidité d’équilibre d’un échantillon à une certaine température et une faible humidité relative ;
Ne gèle pas à basse température (-40°C et moins) ;
Ne peut pas servir de solvant pour les substances ajoutées ;
Donne une bande dans les spectres de résonance magnétique du proton ;
Se déplace avec les macromolécules lors de la détermination du taux de sédimentation, de la viscosité, de la diffusion ;
Existe à proximité du soluté et d’autres substances non aqueuses et possède des propriétés très différentes de celles de l’ensemble de la masse d’eau du système.
Ces caractéristiques fournissent une description qualitative assez complète de l’eau liée. Cependant, son évaluation quantitative basée sur certaines caractéristiques ne garantit pas toujours une convergence des résultats. Par conséquent, la plupart des chercheurs sont enclins à déterminer l’humidité liée par seulement deux des caractéristiques ci-dessus. Par cette définition, humidité liée - c'est de l'eau qui existe à proximité du soluté et d'autres composants non aqueux, qui a une mobilité moléculaire réduite et d'autres propriétés différentes de celles de l'ensemble de la masse d'eau du même système, et qui ne gèle pas à -40°C. Cette définition explique l'essence physique de l'eau liée et permet de la quantifier de manière relativement précise, car l'eau qui ne gèle pas à - 40°C peut être mesurée avec des résultats satisfaisants (par exemple par la méthode PMR ou par calorimétrie). Dans ce cas, la teneur réelle en humidité liée varie en fonction du type de produit.
Les raisons de la rétention d’humidité dans les systèmes complexes sont différentes. Le plus fortement connecté est ce qu'on appelle biologiquement lié eau. Il représente une très petite partie de l’eau des aliments très humides et se trouve, par exemple, dans les crevasses des protéines ou dans les hydrates chimiques. Une autre eau très fortement liée est l'humidité à proximité, représentant une monocouche avec la plupart des groupes hydrophiles du composant non aqueux. L'eau ainsi associée aux ions et aux groupes ioniques est le type d'eau à proximité le plus étroitement lié. Adjacent à la monocouche eau multicouche(eau d'adsorption polymoléculaire), formant plusieurs couches derrière l'eau à proximité. Bien qu'une multicouche soit moins étroitement liée à l'humidité que l'humidité proche, elle est néanmoins suffisamment étroitement liée au composant non aqueux pour que ses propriétés soient donc significativement différentes de celles de l'eau pure. Ainsi, l’humidité liée est constituée d’eau « organique », proche et presque toute l’eau du multicouche.
De plus, de petites quantités d’eau dans certains systèmes cellulaires peuvent avoir une mobilité et une pression de vapeur réduites en raison de la présence d’eau dans les capillaires. La réduction de la pression de vapeur et de l'activité de l'eau (a w) devient significative lorsque les capillaires ont un diamètre inférieur à 0,1 µm. La plupart des produits alimentaires ont des capillaires d'un diamètre de 10 à 100 µm, ce qui, apparemment, ne peut pas affecter de manière significative la diminution de a w dans les produits alimentaires.
Les aliments contiennent également de l’eau retenue dans une matrice macromoléculaire. Par exemple, les gels de pectine et d’amidon, ainsi que les tissus végétaux et animaux contenant de petites quantités de matière organique, peuvent physiquement retenir de grandes quantités d’eau.
Bien que la structure de cette eau dans les cellules et la matrice macromoléculaire ne soit pas précisément établie, son comportement dans les systèmes alimentaires et son importance pour la qualité des aliments sont évidents. Cette eau n'est pas libérée du produit alimentaire, même en cas de force mécanique importante. En revanche, dans les processus de transformation technologique, elle se comporte presque comme de l’eau pure. Par exemple, il peut être retiré une fois séché ou transformé en glace une fois congelé. Ainsi, les propriétés de cette eau en tant qu’eau libre sont quelque peu limitées, mais ses molécules se comportent comme des molécules d’eau dans des solutions salines diluées.
C'est cette eau qui constitue la majeure partie de l'eau des cellules et des gels, et les changements dans sa quantité affectent considérablement la qualité des produits alimentaires. Par exemple, le stockage des gels entraîne souvent une perte de qualité due à la perte de cette eau (appelée synérèse). La conservation par congélation des tissus entraîne souvent une réduction indésirable de la capacité de rétention d'eau pendant la décongélation.
Les tableaux 1 et 2 décrivent les propriétés des différents types d'humidité dans les aliments.
| Propriétés | Gratuit | L'eau dans une matrice macromoléculaire |
| description générale | eau qui peut être facilement éliminée du produit. Eau-eau – les liaisons hydrogène prédominent. Il a propriétés similaires à celles de l'eau dans des solutions salines faibles. A la propriété de libre circulation |
de l'eau qui pourrait être retiré du produit. Eau- liaisons eau-hydrogène prévaloir. Propriétés de l'eau semblable à l’eau dans des solutions salines diluées. La libre circulation est difficile |
| gel ou matrice tissulaire | ||
| Point de congélation | légèrement inférieur à celui de l'eau pure | |
Capacité à être solvant |
grand | |
| Mobilité moléculaire comparée à l'eau pure | un peu moins | |
Enthalpie de vaporisation par rapport à l'eau pure |
sans changements significatifs | |
|
couple sur la teneur totale en humidité des aliments à haute teneur humidité (90% H 2 0),% |
96% | |
Zone isotherme |
l'eau de la zone III est constituée d'eau présente en zones I et II, + eau ajoutée ou retirée à l'intérieur de la zone III |
|
en l'absence de gels et structures cellulaires ceci l'eau est gratuite, bordure inférieure de la zone III flou et dépend de produit et température |
en présence de gels ou structures cellulaires toute eau lié dans une matrice macromoléculaire. Inférieur la limite de la zone III n'est pas claire et dépend du produit et de la température |
|
La raison habituelle gaspillage de nourriture des produits |
vitesse élevée de la plupart des réactions, Croissance microbienne |
|
| Propriétés | Eau liée organiquement | Monocouche | Multicouche |
| description générale | L'eau en tant que partie commune du composant non aqueux | L'eau, qui interagit fortement avec les groupes hydrophiles des composants non aqueux par l'intermédiaire d'une association eau-ion ou eau-dipôle ; eau dans les microcapillaires (d< 0,1 \m) | Eau adjacente à la monocouche et formant plusieurs couches autour du groupe hydrophile de composants non aqueux. Les liaisons eau-eau et eau-soluté-hydrogène prédominent |
| Point de congélation par rapport à l'eau pure | Ne gèle pas à -40 °C | Ne gèle pas à -40 °C | La majeure partie ne gèle pas à -40 "C. Le reste gèle à une température nettement plus basse |
| Capacité à servir de solvant | Non | Non | Assez faible |
| Mobilité moléculaire | Très petit | Beaucoup moins | Moins |
| Enthalpie de vaporisation par rapport à l'eau pure | Fortement agrandi | Augmenté de façon significative | Légèrement agrandi |
Zone isotherme de sorption |
L'eau liée organiquement présente une activité pratiquement nulle et existe donc à l'extrême gauche de la zone. | L’eau de la zone 1 de l’isotherme est constituée d’une petite quantité d’humidité organique avec le reste d’une monocouche d’humidité. La limite supérieure de la zone I n'est pas claire et varie en fonction du produit et de la température | L'eau de la zone 11 est constituée de l'eau présente dans la zone I + de l'eau ajoutée ou retirée au sein de la zone II (humidité multicouche). La limite de la zone II n'est pas claire et varie en fonction du produit et de la température |
| Stabilité des aliments | Auto-oxydation | Stabilité optimale à w = 0,2-0,3 | Si la teneur en eau augmente au-dessus du fond de la zone II, la vitesse de presque toutes les réactions augmente |
Activité d'eau. Isothermes de sorption
On sait depuis longtemps qu'il existe une relation (bien que loin d'être parfaite) entre la teneur en humidité des produits alimentaires et leur sécurité (ou leur détérioration). Par conséquent, la principale méthode pour prolonger la durée de conservation des produits alimentaires a toujours été de réduire la teneur en humidité par concentration ou déshydratation.
Cependant, différents aliments ayant la même teneur en humidité se gâtent souvent différemment. En particulier, il a été constaté que la mesure dans laquelle l'eau est associée à des composants non aqueux est importante : l'eau qui est plus fortement associée est moins capable de soutenir les processus qui détruisent (détériorent) les produits alimentaires, tels que la croissance de micro-organismes et les produits chimiques hydrolytiques. réactions.
Pour prendre en compte ces facteurs, le terme « activité de l’eau » a été introduit. Ce terme caractérise certainement mieux l’effet de l’humidité sur la détérioration du produit que la simple teneur en humidité. Bien entendu, il existe d'autres facteurs (tels que la concentration en 0 2 , le pH, la mobilité de l'eau, le type de substance dissoute) qui, dans certains cas, peuvent avoir une plus grande influence sur la destruction du produit. Cependant, l’activité de l’eau est bien corrélée à la vitesse de nombreuses réactions destructrices et peut être mesurée et utilisée pour évaluer l’état de l’eau dans les aliments et son implication dans les changements chimiques et biochimiques. L'activité de l'eau (a w) est le rapport entre la pression de vapeur de l'eau sur un produit donné et la pression de vapeur sur l'eau pure à la même température. Cette relation est incluse dans la formule thermodynamique de base pour déterminer l'énergie de liaison de l'humidité avec un matériau (équation de Rehbinder) :
ΔF = L = RTln = -RT-lna w
Sur la base de la valeur de l'activité de l'eau (tableau 3), on distingue : les produits à forte humidité (a w = 1,0-0,9) ; produits à humidité intermédiaire (a w = 0,9-0,6) ; produits à faible humidité (a = 0,6-0,0).
Tableau 3 - Activité de l'eau (a w) dans les produits alimentaires
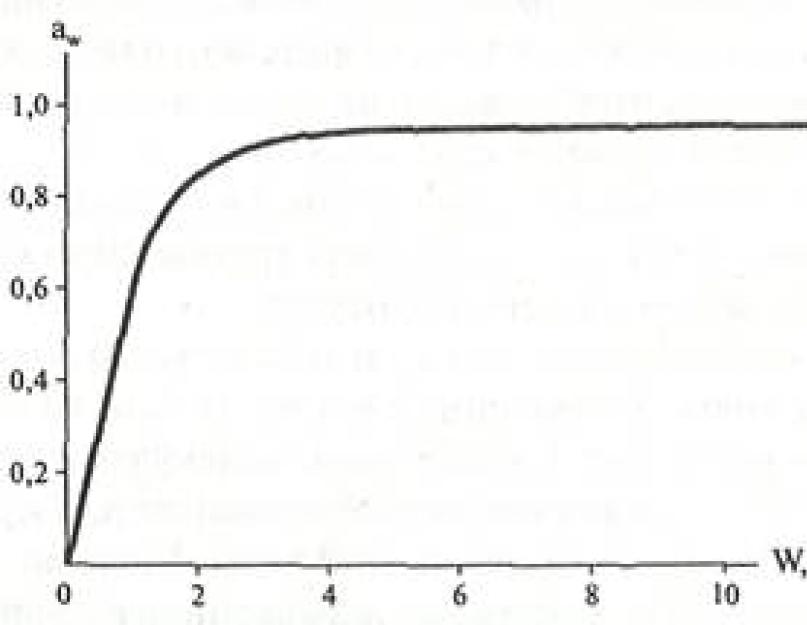
Les courbes montrant la relation entre la teneur en humidité (masse d'eau, g H 2 0 / g MS) d'un produit alimentaire avec l'activité de l'eau qu'il contient à température constante sont appelées isothermes de sorption. Les informations qu'ils fournissent sont utiles pour caractériser les processus de concentration et de déshydratation (la facilité ou la difficulté d'élimination de l'eau étant liée à a w) et pour évaluer la stabilité d'un produit alimentaire. En figue. La figure 10.5 montre l'isotherme de sorption d'humidité pour les produits à forte humidité (dans une large plage de teneur en humidité).

Figure 1. Isotherme de sorption d'humidité pour les produits à forte humidité
Cependant, compte tenu de la présence d'humidité liée, l'isotherme de sorption pour la région de faible teneur en humidité des produits alimentaires présente un plus grand intérêt (Fig. 1).


Figure 2. Isotherme de sorption d'humidité pour la région à faible teneur en humidité des produits alimentaires.
Pour comprendre la signification de l’isotherme de sorption, il est utile de considérer les zones I-III.
Les propriétés de l'eau d'un produit varient considérablement à mesure que l'on passe de la zone I (faible teneur en humidité) à la zone III (forte teneur en humidité). La zone I de l'isotherme correspond à l'eau la plus fortement adsorbée et la plus immobile dans les produits alimentaires. Cette eau est absorbée en raison des interactions polaires eau-ion et eau-dipôle. L'enthalpie de vaporisation de cette eau est bien supérieure à celle de l'eau pure, et elle ne gèle pas à -40°C. Il est incapable d'être un solvant et n'est pas présent en quantité suffisante pour affecter les propriétés plastiques du solide ; elle en fait simplement partie.
L'extrémité très humide de la zone I (la limite des zones I et II) correspond à une monocouche d'humidité. En général, la zone I correspond à une portion extrêmement faible de l’humidité totale d’un produit alimentaire très humide.
L'eau de la zone II est constituée de l'eau de la zone I et de l'eau ajoutée (résorption) pour produire l'eau contenue dans la zone II. Cette humidité forme une multicouche et interagit avec les molécules voisines via des liaisons eau-eau-hydrogène. L'enthalpie de vaporisation de l'eau multicouche est légèrement supérieure à celle de l'eau pure. La majeure partie de cette eau ne gèle pas à -40°C, tout comme l'eau ajoutée à un produit alimentaire dont le taux d'humidité correspond à la limite des zones I et II. Cette eau participe au processus de dissolution, agit comme agent plastifiant et favorise le gonflement de la matrice solide. L'eau des zones II et I représente généralement moins de 5 % de l'humidité totale des aliments très humides.
L'eau de la zone III de l'isotherme est constituée de l'eau qui se trouvait dans les zones I et II et ajoutée pour former la zone III. Dans un produit alimentaire, cette eau est la moins liée et la plus mobile. Dans les gels ou les systèmes cellulaires, il est physiquement lié, de sorte que son flux macroscopique est entravé. À tous autres égards, cette eau a les mêmes propriétés que l’eau dans une solution saline diluée. L'eau ajoutée (ou retirée) pour former la zone III a une enthalpie de vaporisation presque identique à celle de l'eau pure, elle gèle et est un solvant important pour les réactions chimiques et la croissance des micro-organismes. L'humidité ordinaire de la zone III (qu'elle soit libre ou retenue dans une matrice macromoléculaire) représente plus de 95 % de l'humidité totale des matériaux à forte humidité. L'état d'humidité, comme nous le verrons ci-dessous, est important pour la stabilité des produits alimentaires.
En conclusion, il convient de noter que les isothermes de sorption obtenues par ajout d'eau (résorption) à un échantillon sec ne correspondent pas totalement à celles obtenues par désorption. Ce phénomène est appelé hystérésis. Les isothermes de sorption d’humidité pour de nombreux aliments ont une hystérésis. L'ampleur de l'hystérésis, la pente des courbes et les points de début et de fin de la boucle d'hystérésis peuvent varier considérablement en fonction de facteurs tels que la nature du produit alimentaire, la température, le taux de désorption et le niveau d'eau éliminée pendant la désorption.
En règle générale, l'isotherme d'absorption (résorption) est nécessaire pour étudier l'hygroscopique des produits, et l'isotherme de désorption est utile pour étudier les processus de séchage.
Activité de l'eau et stabilité des aliments
Cela dit, il est clair que la stabilité des aliments et l’activité de l’eau sont étroitement liées.
Dans les aliments à faible teneur en humidité, une oxydation des graisses, un brunissement non enzymatique, une perte de substances hydrosolubles (vitamines) et une altération induite par des enzymes peuvent survenir. L'activité des micro-organismes est ici supprimée. Dans les produits ayant une teneur en humidité intermédiaire, divers processus peuvent se produire, notamment ceux impliquant des micro-organismes. Dans les processus se déroulant à une humidité élevée, les micro-organismes jouent un rôle décisif.
L'oxydation des lipides commence à faible aw. À mesure qu'il augmente, le taux d'oxydation diminue approximativement jusqu'à la limite des zones I et II sur l'isotherme, puis augmente à nouveau jusqu'à la limite des zones II et III. Une augmentation supplémentaire de a w réduit à nouveau le taux d'oxydation. Ces changements peuvent s’expliquer par le fait que lorsque l’eau est ajoutée à une matière sèche, elle rencontre d’abord l’oxygène. Cette eau (zone I) lie les hydroperoxydes, interagit avec leurs produits de dégradation et empêche ainsi l'oxydation. De plus, l’eau ajoutée hydrate les ions métalliques qui catalysent l’oxydation, réduisant ainsi leur puissance.
L'assombrissement maximal observé peut s'expliquer par l'apparition d'un équilibre au cours du processus de diffusion, qui est régulé par la valeur de viscosité, le degré de dissolution et le transfert de masse. Lorsque l’activité de l’eau est faible, la diffusion lente des réactifs ralentit la vitesse de réaction. À mesure que la teneur en humidité augmente, une diffusion plus libre accélère la réaction jusqu'à ce que, au sommet de la plage d'humidité, la dissolution des réactifs la ralentisse à nouveau. De même, une concentration plus élevée d’eau ralentit la réaction dans les étapes réversibles au cours desquelles de l’eau se forme.
Des réactions enzymatiques peuvent se produire à une teneur en humidité supérieure à celle de la monocouche, c'est-à-dire quand il y a de l'eau gratuite. Il est nécessaire au transfert du substrat. Compte tenu de cela, il est facile de comprendre pourquoi la vitesse des réactions enzymatiques dépend de a w.
À une w correspondant à l'humidité de la monocouche, il n'y a pas d'eau libre pour le transfert du substrat. De plus, dans un certain nombre de réactions enzymatiques, l'eau elle-même joue le rôle de substrat.
Pour la plupart des bactéries, la valeur limite est a w = 0,9, mais par exemple pour St. aureusa w = 0,86. Cette souche produit une gamme d'entsrotoxines telles que A, B, C, D, E. La plupart des intoxications alimentaires sont associées aux toxines A et D. Les levures et les moisissures peuvent se développer à des niveaux d'activité de l'eau inférieurs.
Pendant le stockage des aliments, l’activité de l’eau affecte la viabilité des micro-organismes. Par conséquent, l’activité de l’eau dans le produit est importante pour éviter sa détérioration microbiologique.
La plupart des détériorations des produits ayant une teneur en humidité intermédiaire sont causées par des levures et des moisissures, et dans une moindre mesure par des bactéries. La levure provoque la détérioration des sirops, des produits de confiserie, des confitures et des fruits secs ; moisissure - viande, confitures, gâteaux, biscuits, fruits secs (tableau 4).
Tableau 4 - Activité de l'eau et croissance microbienne dans les produits alimentaires
| Zone a w | Microorganismes inhibés à une valeur inférieure à cette région | Produits alimentaires typiques de cette région a w |
| 1,00-0,95 | pseudomonas; Escherichia; | fruits, légumes, viandes, poissons, |
| Protée ; Shigella, Klebsiella; | lait, saucisses et pain maison, | |
| Bacille; Clostridium perfingens; | aliments contenant du sucre | |
| un peu de levure | (-40%) et chlorure de sodium (~7%) | |
| 0,95-0,91 | salmonelles, Vibrioparahaemolyticus, Сbotulinum, Serratia Lactobacillus, Pediococcus, certains champignons, levures (Rhodotorula, Pichia) | certains fromages, jambon en conserve, certains jus de fruits concentrés, aliments contenant du sucre (~55%), du chlorure de sodium (~12%) |
| 0,91-0,87 | de nombreuses levures (Candida ; Torulopsis, Hansenula) Micrococcus | saucisson fermenté de type salami, fromages secs, margarine, biscuits en vrac, produits contenant du sucre (65%), du chlorure de sodium (15%). |
| 0,87-0,80 | de nombreux champignons (pénicillium mycotoxigène | la plupart des jus de fruits concentrés, lait concentré sucré, chocolat, sirop, farine, riz, produits fouettés avec une teneur en humidité de 15 à 17 %, gâteaux aux fruits, jambon |
| Pénicilles); Staphylocoque | ||
| Auréus ; majorité | ||
| Saccharomyces; Débaryomyces | ||
| 0,80-0,75 | la plupart des bactéries halophiles, aspergillus mycotoxigènes | confiture, marmelade, fruits surgelés |
| 0,75-0,65 | espèces xérophiles de moisissures (champignons) (Asp. chevalieri; Asp. canidus; Wallemiasebi) Saccharomycesbisporus | mélasse, fruits secs, noix |
| 0,65-0,60 | levure osmophile (Saccharomyces rouxii) ; certaines moisissures (Asp. echinulatus, Monascusbisporus) | fruits secs contenant 15-20% humidité, caramel, miel |
| pas de micro-organismes | pâte avec une teneur en humidité de 12%, épices avec une teneur en humidité de 10% | |
| 0,5 | ||
| 0,4 | pas de micro-organismes | poudre d'oeuf avec humidité -5% |
| 0,3 | pas de micro-organismes | biscuits, craquelins, craquelins avec une teneur en humidité de -3-5% |
| 0,2 | pas de micro-organismes | lait en poudre avec une teneur en humidité de -2-3%, légumes secs avec une teneur en humidité de ~5%, flocons de céréales avec une teneur en humidité de -5%, craquelins |
Un moyen efficace de prévenir la détérioration microbiologique et un certain nombre de réactions chimiques qui réduisent la qualité des produits alimentaires pendant le stockage consiste à réduire l'activité de l'eau dans les produits alimentaires. Pour réduire l'activité de l'eau, des méthodes technologiques telles que le séchage, le séchage, l'ajout de diverses substances (sucre, sel, etc.) et la congélation sont utilisées. Afin d'obtenir l'une ou l'autre activité de l'eau dans le produit, les méthodes technologiques suivantes peuvent être utilisées :
Adsorption - le produit est séché puis humidifié jusqu'à un certain niveau d'humidité ;
Séchage par osmose - les produits alimentaires sont immergés dans des solutions dans lesquelles l'activité de l'eau est inférieure à l'activité de l'eau du produit alimentaire.
Des solutions de sucres ou de sels sont souvent utilisées à cet effet. Dans ce cas, il y a deux contre-courants : le soluté diffuse de la solution vers le produit, et l’eau diffuse du produit vers la solution. Malheureusement, la nature de ces processus est complexe et la littérature ne contient pas suffisamment de données sur cette question.
Pour obtenir l'activité de l'eau requise, divers ingrédients sont ajoutés au produit traité par l'une des méthodes ci-dessus et laissés atteindre un état d'équilibre, car Le processus de séchage seul ne permet souvent pas d’obtenir la consistance souhaitée. En utilisant des humidificateurs, vous pouvez augmenter la teneur en humidité du produit, mais réduire le w. Les humectants potentiels pour les produits alimentaires sont l'amidon, l'acide lactique, les sucres, la glycérine, etc.
Le rôle de la glace dans la stabilité des aliments
La congélation est la méthode la plus courante pour mettre en conserve (conserver) de nombreux aliments. L'effet souhaité est obtenu dans une plus grande mesure par l'effet de la basse température que par la formation de glace. La formation de glace dans les structures cellulaires et les gels alimentaires a deux conséquences importantes :
a) les composants non aqueux sont concentrés dans la phase non congelée (la phase non congelée existe dans les produits alimentaires à toutes les températures de stockage) ;
b) toute l'eau convertie en glace augmente de 9 % en volume.
Pendant la congélation, l'eau se transforme en cristaux de glace de degrés de pureté variables mais assez élevés. Tous les composants non aqueux sont donc concentrés dans une quantité réduite d'eau non congelée. En raison de cet effet, la phase non congelée modifie considérablement les propriétés telles que le pH, l'acidité titrable, la force ionique, la viscosité, le point de congélation, la tension superficielle et le potentiel rédox. La structure de l’eau et les interactions eau-soluté peuvent également changer considérablement.
Ces changements peuvent augmenter les taux de réaction. Ainsi, la congélation a deux effets opposés sur la vitesse des réactions : la basse température en tant que telle la réduira, et la concentration des composants dans l'eau non congelée l'augmentera parfois. Ainsi, un certain nombre d'études ont montré une augmentation du gel du taux de réactions d'assombrissement non enzymatiques qui se produisent au cours de diverses réactions.
Le facteur de possibilité d'augmentation de la vitesse de diverses réactions dans les produits surgelés doit être pris en compte lors de leur stockage, car ce facteur affectera la qualité des produits.
De nombreuses études ont montré qu'une diminution significative de la vitesse de réaction (plus de 2 fois) se produit lorsque les produits alimentaires sont stockés à des températures assez basses (-18°C).
A des températures négatives, assez proches du point de congélation de l'eau (0°C), la proportion de protéines non solubilisées augmente. À une température de -18°C, l'insolubilisation des protéines diminue considérablement, ce qui crée des conditions optimales pour le stockage des produits.
Méthodes de détermination de l'humidité dans les produits alimentaires
Détermination de la teneur en humidité totale
Séchage jusqu'à poids constant.La teneur en humidité est calculée à partir de la différence de masse de l'échantillon avant et après séchage dans une étuve à une température de 100-105°C. Il s'agit de la méthode standard pour déterminer l'humidité. V contrôle techno-chimique des produits alimentaires. Étant donné que la méthode est basée sur le séchage de l’échantillon jusqu’à un poids constant, la méthode nécessite beaucoup de temps pour l’analyse.
Titrage selon la méthode Karl Fischer modifiée. La méthode est basée sur l'utilisation d'une réaction d'oxydo-réduction impliquant de l'iode et du dioxyde de soufre, qui se produit en présence d'eau. L'utilisation de réactifs organiques spécialement sélectionnés permet d'obtenir une extraction complète de l'eau du produit alimentaire, et l'utilisation d'imidazole comme base organique favorise une réaction presque complète. La teneur en humidité du produit est calculée à partir de la quantité d'iode utilisée pour le titrage. La méthode se caractérise par une grande précision et stabilité des résultats (y compris à très faible teneur en humidité) et par la rapidité d'analyse.
Détermination de l'humidité libre et liée
Calorimétrie différentielle à balayage. Si un échantillon est refroidi à une température inférieure à 0 °C, l'humidité libre gèlera, mais pas l'humidité liée. En chauffant un échantillon congelé dans un calorimètre, il est possible de mesurer la chaleur consommée lors de la fonte des glaces. L’eau non gelée est définie comme la différence entre l’eau totale et l’eau glacée.
Méthode thermogravimétrique.La méthode est basée sur la détermination de la vitesse de séchage. Dans des conditions contrôlées, la frontière entre la région de vitesse de séchage constante et la région où cette vitesse diminue caractérise l'humidité liée.
Mesures diélectriques La méthode est basée sur le fait qu'à 0°C les constantes diélectriques de l'eau et de la glace sont approximativement égales. Mais si une partie de l’humidité est liée, ses propriétés diélectriques devraient alors être très différentes de celles de l’eau et de la glace en vrac.
Mesurer la capacité thermique.La capacité thermique de l'eau est supérieure à la capacité thermique de la glace, car. À mesure que la température de l’eau augmente, les liaisons hydrogène se rompent. Cette propriété est utilisée pour étudier la mobilité des molécules d’eau. La valeur de la capacité thermique de l'eau, en fonction de sa teneur en polymères, renseigne sur la quantité d'eau liée. Si, à de faibles concentrations, l’eau est spécifiquement liée, sa contribution à la capacité thermique est alors faible. Dans la région des valeurs d'humidité élevées, elle est principalement déterminée par l'humidité libre, dont la contribution à la capacité thermique est environ 2 fois supérieure à celle de la glace.
La méthode RMN consiste à étudier la mobilité de l’eau dans une matrice stationnaire. En présence d'humidité libre et liée, deux raies sont obtenues dans le spectre RMN au lieu d'une pour l'eau en vrac.
Conclusion
La teneur en eau des produits alimentaires doit être certaine. La diminution ou l'augmentation de la teneur en eau affecte la qualité du produit. Ainsi, la présentation, le goût et la couleur des carottes, des herbes, des fruits et du pain se détériorent avec une diminution de l'humidité, et des céréales, du sucre et des pâtes - avec une humidité croissante. De nombreux produits sont capables d'absorber la vapeur d'eau, c'est à dire qu'ils sont hygroscopiques (sucre, sel, fruits secs, crackers). Étant donné que l’humidité affecte la valeur nutritionnelle des produits alimentaires, ainsi que leur durée de conservation et leurs conditions, elle constitue un indicateur important pour évaluer leur qualité.
La teneur en eau des produits alimentaires ne reste pas constante pendant le transport et le stockage. En fonction des caractéristiques des produits eux-mêmes, ainsi que des conditions environnementales, ils perdent ou s'hydratent. Les produits contenant beaucoup de fructose (miel, caramel), ainsi que les fruits et légumes secs, le thé et le sel de table ont une hygroscopique élevée (capacité à absorber l'humidité). Ces produits sont stockés à une humidité relative ne dépassant pas 65 à 70 %
L’activité de l’eau est l’un des paramètres les plus critiques pour déterminer la qualité et la sécurité des biens consommés quotidiennement. L'activité de l'eau affecte la durée de conservation, la sécurité, la texture et la saveur des produits alimentaires. Il est également vital pour la stabilité des produits pharmaceutiques et cosmétiques. L’activité de l’eau étant si importante, elle doit être mesurée avec précision et rapidité.
En règle générale, la quantité d'eau dans de nombreux produits est normalisée par des normes indiquant la limite supérieure de sa teneur, car non seulement la qualité et la durée de conservation en dépendent, mais également la valeur nutritionnelle des produits.
Bibliographie:
1. L'eau dans les produits alimentaires / Edité par R.B. Canardworth. - Traduction de l'anglais. - M. : Industrie Agroalimentaire, 1980. - 376 s.
2. Ginzburg A.S., Gromov M.A., Krasovskaya G.I. Caractéristiques thermophysiques des produits alimentaires : Manuel. - M. : Agropromizdat, 1990. -287 p.
3. Leistner, L. Technologies barrières : méthodes de transformation combinées qui assurent la stabilité, la sécurité et la qualité des produits alimentaires / L. Leistner, G. Gould. - Traduction de l'anglais. - M. : Institut panrusse de recherche sur l'industrie de la viande. V. M. Gorbatova, 2006. - 236 p.
4. Moik I.B. Tests thermiques et d'humidité des produits alimentaires. Éd. I.A.Rogova-M. : Agropromizdat, 1988. - 303 p.
5. Chimie alimentaire/Nechaev A.P., Traubenberg S.E., Kochetkova A.A. et d'autres. A.P. Nechaeva. 3e édition révisée - Saint-Pétersbourg : GIORD, 2004. – 640 p.
6. Relieur, P.A. Sur les formes de liaison entre l'eau et la matière lors du séchage / Dans le livre. Tous réunion sur l'intensité des processus et l'amélioration de la qualité des matériaux lors du séchage dans les principaux secteurs de l'industrie et de l'agriculture. - M. : Profizdat, 1958. -483 p.
7. http://labdepot.ru/lab/water1.html
8. http://www.upack.by/articles.php
9. http://www.giord.ru/0419205820310.php
10. http://labdepot.ru/lab/water1.html
L'eau est la base de la vie. Quand elle est partie, tout se fige. Mais dès qu'elle devient accessible à tous les êtres vivants, et en grande quantité, la vie recommence à s'épanouir : les fleurs s'épanouissent, les papillons voltigent, les abeilles pullulent... Avec une quantité d'eau suffisante dans le corps humain, des processus de guérison et de restauration se déclenchent. de nombreuses fonctions se produisent également.
Afin d'apporter du liquide au corps, il est nécessaire non seulement de consommer de l'eau sous sa forme pure, ou sous forme de compotes, thés et autres liquides, mais également sous forme de produits contenant de l'eau en quantité maximale.
Aliments riches en eau
La quantité indiquée est une quantité approximative pour 100 g de produit
Caractéristiques générales de l'eau
L'eau est un liquide qui n'a ni goût, ni couleur, ni odeur. Sa composition chimique est l'oxyde d'hydrogène. En plus de l’état liquide, l’eau, comme on le sait, a un état solide et gazeux. Malgré le fait que la majeure partie de notre planète soit recouverte d'eau, la proportion d'eau adaptée au corps n'est que de 2,5 %.
Et si l’on considère que 98,8 % de la quantité totale d’eau douce se trouve sous forme de glace ou cachée sous terre, alors il y a très peu d’approvisionnement en eau potable sur Terre. Et seule une utilisation prudente de cette ressource des plus précieuses nous aidera à sauver des vies !
Besoin quotidien en eau
Quant aux besoins quotidiens en eau de l’organisme, ils dépendent du sexe, de l’âge, de la constitution corporelle, ainsi que du lieu de résidence de la personne. Par exemple, pour une personne vivant sur le littoral, la quantité d’eau consommée peut être réduite par rapport à un habitant du Sahara. Cela est dû au fait qu'une partie de l'eau dont le corps a besoin peut être absorbée par le corps directement à partir de l'humidité de l'air, comme c'est le cas des habitants des zones côtières.
Selon les dernières recherches dans le domaine de la physiologie, la quantité d'eau requise pour une personne est de 30 ml pour 1 kilogramme de poids corporel.
Autrement dit, si le poids d'un adulte est de 80 kg, il doit alors être multiplié par les 30 ml de liquide requis.
Ainsi, on obtient les résultats suivants : 80 x 30 = 2400 ml.
Il s'avère ensuite que pour mener une vie bien remplie, une personne pesant 80 kg doit boire au moins 2 400 ml. liquides par jour.
Le besoin en eau augmente lorsque :
- En cas de température de l'air élevée et de faible humidité. Dans de telles conditions, le corps s'échauffe et, afin d'éviter que la température maximale autorisée pour le corps humain de 41°C ne soit dépassée, la personne commence à transpirer. Ainsi, la température corporelle diminue, mais une grande quantité d'humidité est perdue, qui doit être reconstituée.
- Le besoin en eau augmente avec la consommation d’excès de sel. Dans ce cas, le corps a besoin de plus d'humidité pour normaliser la composition du sang.
- Lorsqu'il souffre de divers types de maladies (par exemple, la fièvre), le corps a besoin de liquide supplémentaire pour le refroidir et pour éliminer rapidement les substances nocives.
Le besoin en eau diminue lorsque :
- Tout d’abord, cela signifie vivre dans un climat rempli de vapeur d’eau. Des exemples de ce type de climat incluent les zones côtières, comme la côte baltique, ainsi que les zones tropicales.
- Deuxièmement, la température de l'air est basse. En hiver, nous voulons toujours boire moins qu'en été, lorsque le corps a besoin d'humidité supplémentaire pour se rafraîchir.
Digestibilité de l'eau
Premièrement, pour une absorption complète de l’eau, une molécule d’eau propre et non pondérée est nécessaire. L'eau destinée à la consommation ne doit pas contenir diverses impuretés nocives. « L'eau lourde » ou deutérium dans sa composition chimique est un isotope de l'hydrogène, mais en raison de sa structure, différente de celle de l'eau ordinaire, tous les processus chimiques dans le corps lorsqu'il est consommé sont plusieurs fois plus lents.
Par conséquent, il convient de rappeler l’eau de fonte, qui est plus légère et plus saine. Cette eau contribue à améliorer le fonctionnement du système cardiovasculaire, accélère les processus de régénération de l'organisme et stimule le métabolisme.
Le deuxième facteur qui influence l’absorption de l’eau est la préparation du corps à ce processus. Les physiologistes ont décrit des exemples où les couches superficielles de la peau, privées d'humidité, empêchaient sa pénétration plus profonde. Un exemple d’une telle injustice est la peau des personnes âgées. Suite à la déshydratation, elle devient flasque, ridée et manque de tonus.
Le troisième facteur influençant la digestibilité de l’eau est l’état de santé humaine. Par exemple, en cas de déshydratation, l’absorption des liquides diminue. (La déshydratation est la perte d'une grande quantité d'humidité par le corps. Chez les adultes, l'indicateur critique est de 1/3 du volume total de liquide dans le corps, chez les enfants jusqu'à 1/5). Dans ce cas, pour lutter contre la déshydratation générale du corps, une perfusion intraveineuse de solution saline est utilisée. La solution a également montré de bons résultats Ringer-Locke. Cette solution, en plus du sel de table, contient du chlorure de potassium, du chlorure de calcium, de la soude et du glucose. Grâce à ces composants, non seulement le volume total de liquide circulant dans le corps est restauré, mais la structure des cloisons intercellulaires est également améliorée.
Propriétés bénéfiques de l'eau et son effet sur le corps
Nous avons besoin d'eau pour que les substances utiles nécessaires au transport vers divers organes et systèmes y soient dissoutes. De plus, l'eau joue un rôle important dans la formation et le fonctionnement de tous les systèmes du corps humain.
Sans eau, tous les processus vitaux seront réduits au minimum. Puisque l'élimination des produits métaboliques est impossible sans la présence d'une quantité suffisante de liquide dans le corps. En cas de pénurie d'eau, le métabolisme en souffre également. C'est le manque d'humidité qui devient responsable de l'excès de poids et de l'incapacité d'atteindre rapidement la forme souhaitée !
L'eau hydrate la peau et les muqueuses, nettoie le corps des déchets et des toxines et constitue la base du liquide articulaire. Avec un manque d'eau, les joints commencent à « grincer ». De plus, l’eau protège les organes internes des dommages, maintient une température corporelle constante et aide à convertir les aliments en énergie.
Interaction de l'eau avec d'autres éléments
Vous connaissez probablement l’expression : « L’eau use les pierres ». Ainsi, l’eau, de par sa nature, est un solvant unique. Il n’existe aucune substance au monde qui puisse contrecarrer l’eau. Dans le même temps, la substance dissoute dans l'eau est pour ainsi dire intégrée à la structure globale de l'eau, occupant l'espace entre ses molécules. Et, malgré le fait que la substance dissoute soit en contact étroit avec l'eau, l'eau n'est pour elle qu'un solvant, capable de délivrer la majeure partie de la substance dans l'un ou l'autre environnement de notre corps.
Signes de manque et d’excès d’eau
Signes de manque d'eau dans le corps
Le premier et le plus important signe d’une faible teneur en eau dans le corps est épaississement du sang. Sans une humidité suffisante, le sang est incapable de remplir ses fonctions. En conséquence, le corps ne reçoit pas suffisamment de nutriments et d'oxygène, et les produits métaboliques ne peuvent pas quitter le corps, ce qui contribue à son empoisonnement.
Mais ce signe ne peut être révélé que par les résultats d'analyses en laboratoire. Par conséquent, seuls les médecins peuvent déterminer la présence d'un manque de liquide sur la base de ce signe. Vous pouvez détecter vous-même les signes suivants de manque d’humidité dans le corps.
Le deuxième signe d’un manque d’eau dans le corps est muqueuses sèches. Dans des conditions normales, les muqueuses doivent être légèrement hydratées. Mais en cas de manque de liquide, les muqueuses peuvent se dessécher et se fissurer.
Le troisième symptôme qui mérite d'être mentionné est sécheresse, pâleur et relâchement cutané, ainsi que la fragilité des cheveux.
La confusion, l'irritabilité et même les maux de tête peuvent également survenir en raison d'une consommation insuffisante de liquides pendant la journée et constituent le quatrième signe le plus important d'un manque de liquide.
L'acné, la langue enduite et la mauvaise haleine sont des signaux importants de manque de liquide et peuvent indiquer un déséquilibre dans l'équilibre hydrique du corps.
Signes d'excès d'eau dans le corps
Si une personne est sujette au surpoids, souffre d'hypertension artérielle et d'un système nerveux labile, et souffre également de transpiration abondante, tout cela indique qu'elle présente des signes d'excès de liquide dans le corps.
Un excès de liquide dans le corps peut entraîner une prise de poids rapide, un gonflement de diverses parties du corps et des troubles du fonctionnement des poumons et du cœur.
Facteurs affectant la teneur en eau corporelle
Les facteurs qui influencent le pourcentage d'eau dans le corps ne sont pas seulement le sexe, l'âge et l'environnement, mais aussi la constitution corporelle. Des études ont montré que la teneur en eau du corps d'un nouveau-né atteint 80 %, celui d'un homme adulte contient en moyenne 60 % d'eau et celui d'une femme, 65 %. Le mode de vie et les habitudes alimentaires peuvent également affecter la teneur en eau de votre corps. Le corps des personnes en surpoids contient beaucoup plus d'humidité que celui des asthéniques et des personnes ayant un poids corporel normal.
Pour protéger l’organisme de la déshydratation, les médecins recommandent de consommer du sel quotidiennement. La norme quotidienne est de 5 grammes. Mais cela ne signifie pas qu’il doit être consommé séparément. Il est inclus dans divers légumes, viandes et plats cuisinés.
Pour protéger le corps de la déshydratation dans des conditions naturelles difficiles, vous devez réduire la transpiration excessive, qui perturbe l'équilibre hydrique. A cet effet, les soldats des forces spéciales ont la composition suivante :
Sel de table (1,5 g) + acide ascorbique (2,5 g) + glucose (5 g) + eau (500 ml)
Cette composition empêche non seulement la perte d'humidité par la transpiration, mais soutient également le corps dans la phase la plus active du maintien de la vie. De plus, cette composition est utilisée par les voyageurs lors de longues randonnées, où la disponibilité d'eau potable est limitée et les charges sont maximales.
Eau et santé
Afin de soutenir votre corps et d’éviter une perte excessive d’humidité, vous devez remplir les conditions suivantes :
- 1 Boire un verre d'eau propre avant chaque repas ;
- 2 Une heure et demie à deux heures après avoir mangé, vous devez également boire un verre d'eau (à condition qu'il n'y ait pas de contre-indications médicales) ;
- 3 Manger des aliments secs peut avoir un impact négatif sur la santé et c'est pourquoi, à titre exceptionnel, il est également recommandé de boire de l'eau pendant ces repas.
L'eau pour perdre du poids
Si vous remarquez que vous commencez à avoir des problèmes de surpoids, suivez les conseils des nutritionnistes et buvez un verre d’eau tiède chaque fois que vous « avez envie de quelque chose de savoureux ». Selon les médecins, nous éprouvons souvent une « fausse faim », sous le couvert de laquelle apparaît une soif élémentaire.
Par conséquent, la prochaine fois que vous vous réveillerez au milieu de la nuit pour aller au réfrigérateur, buvez un verre d'eau tiède, ce qui non seulement vous soulagera de la soif, mais vous aidera également à vous remettre en forme à l'avenir. On pense que le processus de perte de poids est accéléré en consommant la quantité optimale de liquide par jour, calculée à l'aide de la formule donnée ci-dessus.
Pureté de l'eau
Il arrive parfois que « boire » de l’eau devienne dangereux pour la santé, voire la vie. Cette eau peut contenir des métaux lourds, des pesticides, des bactéries, des virus et d'autres contaminants. Tous provoquent des maladies dont le traitement est très difficile.
Par conséquent, afin d’éviter que de tels polluants ne pénètrent dans votre corps, vous devez veiller à la pureté de l’eau. Il existe un grand nombre de méthodes pour cela, allant de la purification de l'eau avec du silicium et du charbon actif, jusqu'aux filtres utilisant des résines échangeuses d'ions, de l'argent, etc.