Значение цветных реакций состоит в том, что они дают возможность обнаружить присутствие белка в биологических жидкостях, растворах и установить аминокислотный состав различных природных белков. Эти реакции применяются как для качественного, так и для количественного определения белка и содержащихся в нем аминокислот. Некоторые реакции присущи не только белкам, но и другим веществам, например, фенол, подобно тирозину, дает розово-красное окрашивание с реактивом Миллона, поэтому проведения одной какой-либо реакции для установления наличия белка не достаточно.
Существует два типа цветных реакций: 1) универсальные – биуретовая (на все белки) и нингидриновая (на все а -аминокислоты и белки); 2) специфические – только на определенные аминокислоты как в молекуле белка, так и в растворах отдельных аминокислот, например реакция Фоля (на аминокислоты, содержащие слабосвязанную серу), реакция Миллона (на тирозин), реакция Сакагучи (на аргинин) и др.
При проведении цветных реакций на белки и аминокислоты необходимо предварительно составить следующую таблицу:
Цветные реакции на белки (качественные реакции)
Цветные реакции на белки Опыт 1. Биуретовая реакция.
Биуретовая реакция – качественная на все без исключения белки , а также продукты их неполного гидролиза , которые содержат не менее двух пептидных связей .
Принцип метода. Биуретовая реакция обусловлена присутствием в белках пептидных связей (- СО – NH -), которые в щелочной среде образуют с сульфатом меди (ІІ) окрашенные в красно-фиолетовый цвет медные солеобразные комплексы . Биуретовую реакцию дают также некоторые небелковые вещества, например биурет (NH 2 -CO-NH-CO-NH 2), оксамид (NH 2 CO-CO-NH 2), ряд аминокислот (гистидин , серин , треонин , аспарагин ).
Биуретовая реакция с глицином
Порядок выполнения работы.
К 1 мл исследуемого 1% раствора белка добавляют равный объем 10 % раствора гидроксида натрия (NaOH) щелочи и затем 2-3 капли 1 % раствора сульфата меди (CuSO 4). разбавленного, почти бесцветного раствора медного купороса.
При положительной реакции появляется фиолетовая окраска с красным либо синим оттенком.
Опыт 2. Реакция на «слабосвязанную серу».
Принцип метода. Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Порядок выполнения работы.
В пробирку наливают 1 мл неразбавленного куриного белка, прибавляют 2 мл 20%-го раствора гидроксида натрия. Смесь осторожно кипятят (чтобы смесь не выбросило).
При этом выделяется аммиак, который обнаруживается по посинению влажной лакмусовой бумажки, поднесенной к отверстию пробирки (не касаться стенки). Образующийся незначительный осадок растворяется при кипении, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):


Химизм реакции:

|
черный осадок |
В пробирку наливают 1 мл. неразбавленного куриного белка добавляют 2 мл. концентрированного раствора щелочи, кладут несколько кипятильников. К горячему раствору добавляют раствор плюмбита натрия – образуется желто-бурое или черное окрашивание. (Плюмбит натрия готовят следующим образом: к 1 мл уксуснокислого свинца добавляют раствор щелочи по каплям до растворения образующего вначале осадка гидроксида свинца).
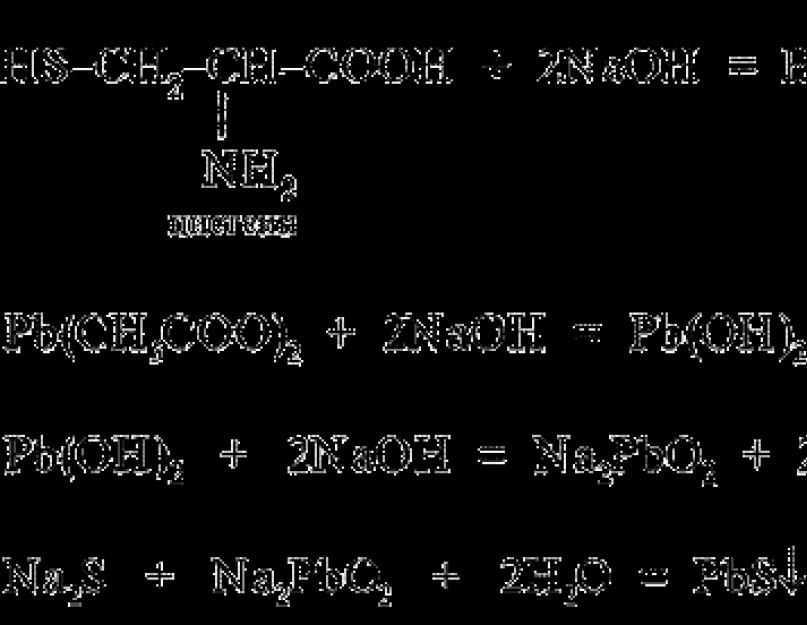
При наличии в молекуле белка серосодержащих аминокислот (цистина, цистеина) из этих аминокислот постепенно отщепляется сера в виде иона в степени окисления – 2, наличие которого и обнаруживается ионом свинца, образующим с ионом серы черный нерастворимый сульфид свинца:
Pb(CH 3 COO) 2 + 2NaOH Pb(OH) 2 + 2 CH 3 COONa,
Pb(OH) 2 + 2NaOH Na 2 PbO 2 + H 2 O,
Na 2 S + Na 2 PbO 2 + 2H 2 O PbS + 4NaOH.
Опыт 3. Ксантопротеиновая реакция белков.
Принцип метода. Эта реакция используется для обнаружения a-аминокислот, содержащих ароматические радикалы. Тирозин, триптофан, фенилаланин при взаимодействии с концентрированной азотной кислотой образуют нитропроизводные, имеющие желтую окраску. В щелочной среде нитропроизводные этих a-аминокислот дают соли, окрашенные в оранжевый цвет. Желатин, например, не содержащий ароматических аминокислот, не дает ксантопротеиновой пробы.
Порядок выполнения работы.
К 1 мл 10 %-го раствора белка куриного яйца добавляют 0,5 мл концентрированной азотной кислоты. В результате коагуляции белка в содержимом пробирки образуется белый осадок или помутнение. При нагревании раствор и осадок окрашиваются в ярко-желтый цвет. При этом осадок почти полностью растворяется в результате гидролиза. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия (до появления оранжевой окраски раствора).
Рассмотрим механизм ксантопротеиновой реакции по радикалу тирозина:


Химизм реакции :

Оформление опыта: сделать вывод и написать уравнение реакции.
Опыт 4. Реакция Адамкевича (на присутствие в белках триптофана).
Принцип метода. Белки, содержащие триптофан, в присутствии глиоксиловой и серной кислот дают красно-фиолетовое окрашивание. Реакция основана на способности триптофана взаимодействовать в кислой среде с альдегидами глиоксиловой кислоты (являющейся примесью к концентрированной уксусной кислоте) с образованием окрашенных продуктов конденсации. Реакция протекает по уравнению:

Желатин не дает этой реакции, т.к. он не содержит триптофана. Окраска возникает за счет реакции триптофана с глиоксиловой кислотой, всегда присутствующей в уксусной кислоте в виде примеси.
Эту же реакцию на триптофан можно провести, используя вместо уксусной кислоты формальдегид 2,5%-ный раствор концентрированной H 2 SO 4. Раствор перемешать и через 2-3 мин. добавить при взбалтывании 10 капель 5%-ного нитрита натрия. Развивается интенсивно-фиолетовое окрашивание, на этом основан принцип метода реакции.
Порядок выполнения работы.
В пробирку наливают несколько капель неразбавленного белка и прибавляют 2 мл. ледяной уксусной кислоты и несколько капель глиоксиловой кислоты. Смесь слегка нагревают до растворения образующегося осадка, охлаждают и, сильно наклонив пробирку, осторожно по стенке приливают концентрированную H 2 SO 4 так, чтобы обе жидкости не смешивались.
Через 5-10 минут на границе раздела двух слоев наблюдают образование красно-фиолетового кольца.
Опыт 5. Нингидриновая реакция.
Принцип метода. a-Аминокислоты реагируют с нингидрином, образуя сине-фиолетовый комплекс (пурпур Руэманна), интенсивность окраски которого пропорциональна количеству аминокислоты. Реакция идет по схеме:

Химизм реакции :


Реакция с нингидрином используется для визуального обнаружения a-аминокислот на хроматограммах (на бумаге, в тонком слое), а также для колориметрического определения концентрации аминокислот по интенсивности окраски продукта реакции.
Продукт этой реакции содержит в своем составе радикал (R) исходной аминокислоты, который обусловливает различную окраску: голубую, красную, и т.д. соединений, возникающих при реакции аминокислот с нингидрином.
В настоящее время нингидриновая реакция широко используется как для открытия отдельных аминокислот, так и для определения их количества.
Порядок выполнения работы.
В пробирку наливают 1 мл 1-10%-го разбавленного раствора белка куриного яйца и 1-2 мл 1%-го раствора нингидрина в ацетоне. Содержимое пробирки перемешивают и в течение 2-3 мин осторожно нагревают на водяной бане до появления сине-фиолетового окрашивания, свидетельствующее о присутствии в белке α -аминокислот.
Оформление опыта: сделать вывод и написать уравнение реакции.
Опыт 6. Реакция Сакагучи.
Принцип метода. Эта реакция на аминокислоту аргинин основана на взаимодействии аргинина с a-нафтолом в присутствии окислителя. Ее механизм еще полностью не выяснен. По-видимому, реакция осуществляется по следующему уравнению:

Поскольку производные хинониминов (в данном случае нафтохинона), у которых водород иминогруппы –NH– замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона, то, по-видимому, оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именно производного нафтохинонимина. Не исключена, однако, вероятность образования еще более сложного соединения за счет дальнейшего окисления оставшихся NH-групп аргининового остатка и бензольного ядра a-нафтола:
Порядок выполнения работы.
К 2 мл. 1%-го разбавленного раствора белка куриного яйца добавляют 2 мл. 10%-го гидроксида натрия (NaOH) и несколько капель 0,2%-ного спиртового раствора α -нафтола. Содержимое пробирки хорошо перемешивают. Затем приливают 0,5 мл. гипобромита натрия (NaBrO) или гипохлорита натрия (натрий хлорноватистокислый – NaOCl), перемешивают. Тотчас появляется красное, постепенно усиливающееся окрашивание.
Немедленно добавляют 1 мл 40%-го раствора мочевины для стабилизации, быстро развивающегося оранжево-красного окрашивания.
Эта реакция характерна для соединений, содержащих остаток гуанидина
NH = C –NH 2 ,
и указывает на присутствие в белковой молекуле аминокислоты-аргинина:
NH = C –NH – (CH 2) 3 –CH –COOH
Оформление опыта: сделать вывод и написать уравнение реакции.
Цветные реакции на белки
Присутствие белков в биологических объектах или растворах можно определить с помощью цветных реакций, протекание которых обусловлено наличием в белке специфических групп и пептидных связей.
Реактивы: водный раствор яичного белка (белок одного куриного яйца отделяют от желтка, растворяют в 15–20-кратном объеме дистиллированной воды, затем раствор фильтруют через марлю, сложенную в 3–4 слоя, и хранят в холодильнике;10 %-й раствор гидроксида натрия; 30 %-й раствор гидроксида натрия; 1 %-ный раствор сульфата меди; 1 %-й раствор ацетата свинца; концентрированная азотная кислота; 0,5 %-й раствор нингидрина.
Оборудование : пробирки; водяная баня или спиртовка.
Задание 1. Биуретовая реакция.
В щелочной среде белки, а также продукты их гидролиза – пептиды дают фиолетовое или красно-фиолетовое окрашивание с солями меди. Реакция обязана наличию пептидных связей в белках:
Интенсивность окраски зависит от длины полипептида.
Ход работы
- В пробирку налейте 5 капель раствора яичного белка, затем 10 капель 10 %-го раствора щелочи.
- Добавьте 1–2 капли раствора сульфата меди, смесь перемешайте. Появляется красно-фиолетовое окрашивание.
Задание 2. Ксантопротеиновая реакция.
Реакция характерна для некоторых ароматических аминокислот (фенилаланина, тирозина, триптофана), а также для пептидов, их содержащих. При действии азотной кислоты образуется нитросоединение желтого цвета. Далее нитропроизводные могут реагировать со щелочью с образованием натриевой соли, имеющей желто-оранжевое окрашивание:

Ход работы
Данную работу необходимо выполнять в вытяжном шкафу, соблюдая особую осторожность!
- В пробирку налейте 5 капель раствора яичного белка и ОСТОРОЖНО по стенке прибавьте 3–4 капли концентрированной азотной кислоты.
- Смесь осторожно нагрейте. Выпадает осадок, который окрашивается в желтый цвет.
- После охлаждения в пробирку ОСТОРОЖНО по стенке прилейте 10 капель 30 %-го раствора NaOH, желтая окраска переходит в оранжевую.
Задание 3 . Реакция на серусодержащие аминокислоты (реак ция Фоля).
В остатках серусодержащих аминокислот цистеина и цистина сера при щелочном гидролизе отщепляется, образуя сульфиды. Сульфиды, взаимодействуя с ацетатом свинца, образуют осадок сульфида свинца черного или буро-черного цвета.

Ход работы
- В пробирке смешайте 5 капель раствора яичного белка, 5 капель 30 %-го раствора щелочи и 2 капли раствора ацетата свинца.
- Смесь осторожно нагрейте на спиртовке до кипения и кипятите. Через некоторое время появляется буровато-черное или черное окрашивание.
Задание 4 . Нингидриновая реакция.
Реакция характерна для аминогрупп в α-положении и обусловлена наличием α-аминокислот в молекуле белка. При нагревании белка с водным раствором нингидрина аминокислоты окисляются и распадаются, образуя двуокись углерода, аммиак и соответствующий альдегид. Восстановленный нингидрин конденсируется с аммиаком и окисленной молекулой нингидрина, образуя соединение фиолетово-синего цвета:

Ход работы
В пробирку вносят 5 капель 1 %–го раствора яичного белка, добавляют по 3 капли 0,5 %-го раствора нингидрина и нагревают до кипения. Через 2–3 минуты появляется розовое, красное, а затем сине-фиолетовое окрашивание.
Оформление результатов
Оформите проведенные исследования в виде таблицы.
Цель работы: доказать присутствие в биологических объектах таких важных органических соединений, как белки, липиды, углеводы
Ход работы:
1 Определение глюкозы в виноградном соке
К 2 см3 виноградного сока добавьте 1 см3 раствора едкого натра и 3 капли раствора сульфата меди. Нагрейте до кипения.
Аналитический эффект: наблюдается образование желтого осадка Cu(OH)2, который при дальнейшем нагревании переходит в красный осадок Cu2О.
2 Реакция крахмала с йодом
К 2 мл раствора крахмала прибавляют 1–2 капли раствора Люголя. Раствор окрашивается в синий цвет. Затем нагревают. Окраска исчезает, но окраска вновь появляется при охлаждении.
3. Физико-химические свойства жиров
Взять 2 пробирки. В первую налить 2мл дистиллированной воды, во вторую – спирта. В каждую пробирку налить по 5 капель растительного масла. Все пробирки хорошо взболтать и отметить растворение жира в разных веществах.
4. Эмульгирование жиров
Взять 2 пробирки. В каждую из них налить по 3 мл дистиллированной воды и свежее растительное масло. Во вторую пробирку добавить несколько капель 10% раствора соды Na2CO3. Все пробирки закрывают, тщательно взбалтывают. Оставляют на 5 мин стоять и наблюдают стойкость эмульсии.
5. Определение непредельности жира
В пробирку внести 0,5-1г масла, прилить 2 капли КМnО4 и тщательно взболтать. Происходит обесцвечивание перманганата.
6. Биуретовая реакция на определение пептидной связи
В пробирку внести 5 капель 1%-ного раствора яичного белка, 3 капли 10-%- ного раствора NaOH и одну каплю 1%-ного раствора CuSO4 и перемешать. Содержимое пробирки приобретает сине-фиолетовое окрашивание.
7. Ксантопротеиновая реакция
К 5 каплям 1%-ного раствора яичного белка приливают 3 капли концентрированной азотной кислоты (осторожно!) и нагревают. Появится осадок желтого цвета. После охлаждения в пробирку добавьте 5-10 капель 10%-ного раствора NaOH до появления оранжевого окрашивания (оно связано с образованием натриевой соли этих нитросоединений).
8. Свертывание белков при нагревании
В пробирку нальем немного раствора белка. Нагреем раствор до кипения. Раствор мутнеет, белок выпадает в виде хлопьев. Свертывание белков при кипении - процесс необратимого осаждения, белковые молекулы меняют свою структуру.
9. Осаждение белков солями тяжелых металлов, спиртом, серной кислотой
В две пробирки приливаем раствор белка. В первую пробирку добавляют раствор сульфата меди (II), во вторую – раствор нитрата серебра. В обеих пробирках выпадают осадки. Соли тяжелых металлов осаждают белки из растворов, образуя с ними нерастворимые в воде солеобразные соединения.
К раствору белка прибавляем немного этилового спирта. Раствор мутнеет. При действии спирта происходит денатурация белка – разрушение его структуры.
К раствору белка прибавляем немного серной кислоты. Выпадает осадок. При действии серной кислоты происходит денатурация белка – разрушение его структуры.
Отчет по лабораторной работе оформите в виде таблицы (каждый опыт отдельно)
Исходные веществаЧто делали?Что наблюдали?Выводы, уравнения реакцииДемонстрационный опыт № 5, доказывающий наличие белка в клетке. Для проведения этого опыта я приготовила муку. Муку помещаем в марлю и хорошо промываем тесто в стакане с водой. (Белое, тягучее (растянуть) и клейкое (потрогать) вещество (масса)). Эта тягучая клейкая масса – клейковина. Она сходна по составу с белком куриного яйца и называется растительным белком. Аккуратно выньте комочек теста и осмотрите его развернув марлю. Потрогайте его пальцем. Белок – клейковина содержится в клетках пшеницы, ржи и других злаков. Вывод: в состав растений входит белок. Роль белка: Для питания зародыша при прорастании. Благодаря этому белку (клейковине) человек может из муки получать тесто и печь хлеб и пироги.
Слайд 10 из презентации «Биология 5 класс»Размеры: 720 х 540 пикселей, формат: .jpg. Чтобы бесплатно скачать слайд для использования на уроке, щёлкните на изображении правой кнопкой мышки и нажмите «Сохранить изображение как...». Скачать всю презентацию «Биология 5 класс.pptx» можно в zip-архиве размером 1368 КБ.
История биологии
«Хищник пума» - Вот потому-то человек начал уничтожать Пуму. Численность животных сократилась из-за разрушения мест обитания (вырубка лесов). За добычу пум даже выплачивали премии. Живут пумы около 15 лет. Вес до 90 килограмм. Пума отлично лазает по деревьям и обрывам. Длина взрослой пумы до кончика хвоста достигает 2,5 метров.
«Класс пресмыкающиеся» - Окраска змей покровительственная, маскирующая. Поясничный, - Почему лягушек называют амфибиями? Все тело ящерицы покрыто сухой кожей без желез. Температура тела непостоянная, зависит от температуры окружающей среды. Ушные отверстия, прикрытые барабанной перепонкой и кожей. Известковой скорлупой (черепахи, крокодилы).
«Белки вещество» - Например, коллаген сухожилий, кератин волос. Например, актомиозин. Например, гемоглобин. Необратимая. Используются организмом для движения. Функции белков. Например, белок гликопротеин. Ферментативная Строительная Транспортная Сократительная Регуляторная Пищевая Защитная Энергетическая Рецепторная. Определяют способность клетки узнавать чужеродные антигены.
«Развитие органического мира» - Содержание кислорода в атмосфере постепенно повышалось. ПАЛЕОЦЕНОВАЯ ЭПОХА (третичный период). Африка "врезалась" в Европу и Азию, в результате чего возникли Альпы. Юрский период. В конце периода началось новое оледенение. Около 1350 млн. лет назад отмечены представители низких грибов. Развитие органического мира.
«Покрытосеменные растения» - Составить кроссворд: «Покрытосеменные растения» Нарисовать рисунки, подобрать картинки по теме. Ветреница вильчатая. Встречается в пресных водоемах Австралии. Венерин башмачок. Монстера. Пищевое Лекарственное Кормовое Декоративное Строительное Техническое Топливо Ядовитые. Покрытосеменные растения Челябинской области, занесенные в Красную Книгу.
Ход работы:
Оформите в тетради(в клетку) проведённый опыт:
Опыт « Определение белка в клетке».
Цель: научиться…..(продолжите).
Оборудование: стаканчик с водой, мука в марле, ножницы.
Ход работы:
1. Опустите завёрнутую в марлю муку в стакан с водой на полминуты. Выньте, разрежьте нитку на марле, разверните и потрогайте полученное тесто пальчиком. Напишите в этом пункте
что наблюдаете? (« Если мокрую муку потрогать, то на ощупь она будет …?.... , …?.....»)
2. Найдите в учебнике: какое вещество обладает такими качествами? Сделайте вывод: какое органическое вещество вы обнаружили. («Вывод: это вещество - ….?.... (…….) .»)
3. Найдите в учебнике и запишите в этом пункте значение в клетке вашего органического вещества. (« Значение: …….. .»)
Оформите в тетради(в клетку) проведённый опыт:
Опыт « Определение белка в клетке».
Цель: научиться…..(продолжите).
Оборудование: стаканчик с водой, мука в марле, ножницы.
Ход работы:
1. Опустите завёрнутую в марлю муку в стакан с водой на полминуты. Выньте, разрежьте нитку на марле, разверните и потрогайте полученное тесто пальчиком. Напишите в этом пункте
что наблюдаете? (« Если мокрую муку потрогать, то на ощупь она будет …?.... , …?.....»)
2. Найдите в учебнике: какое вещество обладает такими качествами? Сделайте вывод: какое органическое вещество вы обнаружили. («Вывод: это вещество - ….?.... (…….) .»)
3. Найдите в учебнике и запишите в этом пункте значение в клетке вашего органического вещества. (« Значение: …….. .»)
По теме: методические разработки, презентации и конспекты
Презентация содержит материал для интегрированного урока химии и биологии по теме"Белки, их состав, свойства и биологические функции". На слайдах представлены вопросы для самостоятельной работы учащих...
Биосинтез белков в живой клетке
Задачи и цели урока:Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа биосинтеза белка – трансляцию и транскрипцию. Задачи: Вспомнить значение б...
Конспект урока по технологии проблемного обучения "Биосинтез белка в живой клетке"
Конспект урока "Биосинтез белка в живой клетке" разработан с использованием технологии проблемного обучения. На уроке учащиеся повторяют свойства генетического кода, процесс транскрипции, знакомятся с...